
| A. | 原子半径:A>B | |
| B. | 失电子的能力:C<D | |
| C. | 简单气态氢化物的稳定性:B>E | |
| D. | 元素C、D、E的最高价氧化物对应的水化物两两之间能发生反应 |
分析 短周期的A、B、C、D、E物种元素,原子序数依次增大,元素A的气态氢化物和A的最高价氧化物对应的水化物反应生成盐,则A是N元素;B、E为同主族元素,B元素原子最外层电子数是次外层的3倍,元素最外层电子数不超过8个,第一电子层为最外层时不超过2个,则B是O元素,E是S元素;C是短周期中与水反应最激烈的金属元素,则C是Na元素;A、D最外层电子数相差2,而且原子序数比Na大,则D是Al元素,据此分析.
解答 解:短周期的A、B、C、D、E物种元素,原子序数依次增大,元素A的气态氢化物和A的最高价氧化物对应的水化物反应生成盐,则A是N元素;B、E为同主族元素,B元素原子最外层电子数是次外层的3倍,元素最外层电子数不超过8个,第一电子层为最外层时不超过2个,则B是O元素,E是S元素;C是短周期中与水反应最激烈的金属元素,则C是Na元素;A、D最外层电子数相差2,而且原子序数比Na大,则D是Al元素;
A.同一周期元素,原子半径随着原子序数增大而减小,所以原子半径A>B,故A正确;
B.同一周期元素,金属元素的失电子能力随着原子序数增大而减弱,则失电子的能力:C>D,故B错误;
C.非金属性越强,其氢化物的稳定性越强,非金属性:B>E,则简单气态氢化物的稳定性:B>E,故C正确;
D.C是Na元素、D是Al元素、E是S元素,C的最高价氧化物的水化物呈强碱性、D的最高价氧化物的水化物呈两性、E的最高价氧化物的水化物呈强酸性,所以这三种元素最高价氧化物的水化物两两能相互反应,故D正确;
故选B.
点评 本题考查原子结构和元素性质,侧重考查原子结构、物质性质,明确物质的性质是解本题关键,注意把握元素周期律的内容以及非金属性的比较方法.


科目:高中化学 来源: 题型:选择题
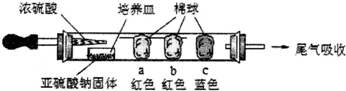
| A. | 本实验是利用强酸制弱酸原理制得SO2气体 | |
| B. | 棉球a沾有品红试液,用以验证SO2的漂白性 | |
| C. | 棉球b红色褪去,说明SO2是酸性氧化物,与水反应能生成亚硫酸 | |
| D. | 棉球C沾有含石蕊的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 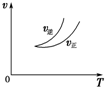 可判断正反应为放热反应 | |
| B. | 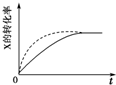 虚线表示可能使用了催化剂或是加压 | |
| C. | 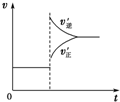 若正反应的△H<0,可表示升高温度使平衡向逆反应方向移动 | |
| D. | 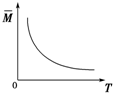 气体平均相对分子质量随温度变化情况,可推知正反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.下如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.下如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质与SN2互为同素异形体 | |
| B. | 该物质的分子中既有极性键又有非极性键 | |
| C. | 该物质可能是离子化合物 | |
| D. | 该物质的一个分中含有9个N-S键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应在常温下一定很容易发生 | |
| B. | 化学反应一定既伴随着物质变化又伴随着能量变化 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 反应物所具有的总能量高于生成物所具有的总能量的反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
| A. | X的最高价氧化物的水化物碱性比Y的弱 | |
| B. | Y既可以和酸反应又可以和碱反应,且化合价变化相同 | |
| C. | 常温下,Z单质可以与L的氢化物溶液反应置换出L单质 | |
| D. | X、M分别与Q形成的化合物中所含化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与乙烯互为同系物 | |
| B. | 其具有6种同分异构体 | |
| C. | 其一氯代物一共有12种 | |
| D. | 该物质的系统命名的名称为“1-丁烯” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2 | B. | NH3 | C. | Cl2 | D. | HI |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCN 与KOCN中氮元素的化合价均为-3价 | |
| B. | 氰酸盐进一步被氧化的产物之一是无毒的N2 | |
| C. | OCN-与CN-中σ键与π键个数比均为1:2 | |
| D. | 完全处理含0.1 mol CN-的废水,理论上需要消耗Cl2的体积为5.6L(标准状况下) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com