
| A、Cl2的水溶液可以导电,说明Cl2是电解质 |
| B、在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si |
| C、向淀粉碘化钾的溶液中加入氯水,溶液变为蓝色,说明Cl2的氧化性强于I2 |
| D、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液,溶液褪色,说明BaCl2溶液有酸性 |


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
| A、3a% |
| B、(100-2a)% |
| C、20% |
| D、1-3a% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol Fe3+和28g的Si都含有NA个原子 |
| B、标况下,22.4 L的空气中含有NA个单质分子 |
| C、1mol Cl2参加反应时,转移的电子数可能是2NA个 |
| D、含有NA个Na的金属钠,投入1L H2O中,所得溶液的物质的量浓度为1 mol/l |
查看答案和解析>>
科目:高中化学 来源: 题型:
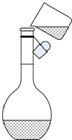 实验室中需要配制500mL0.10mol/L的NaOH溶液.回答下列问题.
实验室中需要配制500mL0.10mol/L的NaOH溶液.回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在常温常压下,11.2L H2含有的分子数为0.5NA |
| B、32g O2所含原子数目为2NA |
| C、1mol HCl含有的电子数为2NA |
| D、在标准状况下,22.4L H2O含有的质子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,48gO3含有的原子数为3NA |
| B、1L 1mol/L 的CH3COOH溶液中含有的CH3COO-的数目为NA |
| C、11.2 L氧气所含的原子数为NA |
| D、5.6g铁与盐酸完全反应时失去的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温时Ka(HF)>Ka(HCN),则相同条件下NaF溶液的pH比NaCN溶液大 |
| B、0.1 mol?L-1NH4Cl溶液:c(NH4+)=c(Cl-) |
| C、同浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3?H2O;c(NH4+)由大到小的顺序是:①>②>③>④ |
| D、物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三者浓度相同时,pH大小顺序为③>②>① |
| B、三者浓度相同时,稀释相同倍数,pH变化最大的为② |
| C、三者的pH均为9时,物质的量浓度的大小关系为③>②>① |
| D、三者浓度相同时,分别加入同体积同浓度的盐酸后,pH最大的是① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com