
(10分)图中字母所代表的物质均为中学化学常见物质。其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料;常温下C、D、H为气体单质。单质E、M、N为金属,N是地壳中含量最大的金属元素。Y是红褐色沉淀。这些物质在一定条件下存在如下转化 关系,其中有些反应物或生成物已经略去。试回答下列问题:
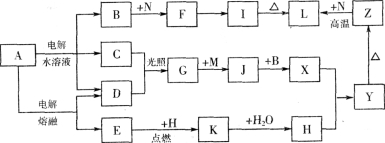
(1)Z→L反应的名称是 。
(2)K的电子式为 。
(3) 写出B→F的离子方程式 。
(4) 写出K与CO2反应的化学方程式 。
(5) Y与NaClO和B的混合溶液作用,是制备绿色水处理剂(Na2MO4)的一种方法,请写出该反应的离子方程式 。
(1)铝热反应 (2) 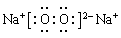 (3)2Al+2OH-+2H2O=2AlO2-+3H2↑
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)2Na2O2+2CO2=2Na2CO3+O2 ;(5)2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
【解析】
试题分析:常温下C、D、H为气体单质.单质E、M、N为金属,N是地壳中含量最大的金属元素,可知N为铝.Y是红褐色沉淀,Y为氢氧化铁,则Z为Fe2O3,L为Al2O3,I为Al(OH)3,C、D在光照条件下反应生成G,则应为Cl2和H2的反应,G为HCl,其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料,A为氯化钠,电解饱和食盐水生成H2,Cl2,和NaOH,则B为NaOH,C为H2,D为Cl2,E为电解NaCl的产物,应为Na,H为氧气,K为Na2O2;根据X与氧气反应生成氢氧化铁,则X为Fe(OH)2,J为FeCl2,M为Fe;则
(1)Z是氧化铁,N是铝,则Z→L反应的名称是铝热反应;
(2)K是过氧化钠,过氧化钠为离子化合物,化合物中含有过氧键,电子式为: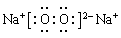 ;
;
(3)铝既能与强酸反应,也能与强碱反应,分别生成盐和水,与氢氧化钠溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)过氧化钠与二氧化碳反应生成碳酸钠和氧气,方程式为:2Na2O2+2CO2=2Na2CO3+O2;
(5)NaClO在碱性条件下具有强氧化,可进一步氧化2Fe(OH)3,反应的离子方程式为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O。
考点:考查无机框图题的推断


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015届甘肃省天水市高二上学期期中考试化学(文)试卷(解析版) 题型:选择题
通常听说的“白色污染”是指
A.聚乙烯等白色塑料垃圾 B.石灰窑的白色粉尘
C.冶炼厂的白色烟尘 D.白色建筑废料
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:填空题
(12分)(1)环境专家认为可以用金属铝将水体中的NO 转化为N2,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH
转化为N2,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH 、Al(OH)3、NO
、Al(OH)3、NO 、N2,写出反应的离子方程式 。
、N2,写出反应的离子方程式 。
(2)我国首创的海洋电池以海水为电解质溶液,电池总反应为:4Al+3O2+6H2O=4Al(OH)3。电池正极的电极反应式为 。
(3)已知:4Al(s)+3O2(g)=2Al2O3(g) △H=-2834.9kJ/mol
Fe2O3(s)+ C(s)=
C(s)=  CO2(g)+2Fe(s) △H=+234.1kJ/mol
CO2(g)+2Fe(s) △H=+234.1kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
写出铝与氧化铁发生铝热反应的热化学方程式 。
(4)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mol,pH=14的溶液,然后2mol/L盐酸滴定,可得沉淀质量与消耗的盐酸体积关系如下图:则反应过程中产生氢气的总体积为 L(标准状况)

查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
下列各组离子在指定条件下能大量共存的是
①漂白粉的水溶液中:Fe2+、Cl—、Ca2+、Na+ ②滴加石蕊试液呈红色的溶液:K+、NH4+、Cl—、S2— ③能够与金属Cu常温下反应放出气体的溶液:Fe3+、Al3+、SO42-、K+ ④常温下pH =2的溶液中:NH4+、Na+、Cl—、Cu2+ ⑤无色溶液中:K+、CH3COO—、HCO3—、MnO4—
A、②③ B、①③ C、③④ D、①⑤
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A、晶体硅具有半导体性质,可用于生产光导纤维
B、H2O2是一种绿色氧化剂,可与酸性高锰酸钾作用产生O2
C、铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸
D、铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料
查看答案和解析>>
科目:高中化学 来源:2015届湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列过程最终无沉淀产生的是( )
A.过量氨气通入Al2(SO4)3溶液
B.CO2通入CaCl2溶液
C.少量SO2通入BaCl2溶液后再通入过量Cl2
D.过量CO2通入Na2SiO3溶液
查看答案和解析>>
科目:高中化学 来源:2015届湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是
A.Na2FeO4既是氧化产物又是还原产物
B.Na2O2只作氧化剂
C.O2是还原产物
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015届湖南省衡阳市五校高三11月联考化学试卷(解析版) 题型:选择题
以下物质间的转化通过一步反应不能实现的是
A.HCl →Cl2→HClO→NaClO
B.Na→Na2O2→Na2CO3→NaHCO3
C.Al→NaAlO2 →Al(OH)3→Al2O3
D.Si→SiO2→H2SiO3→Na2SiO3
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高三上学期第三次模拟考试化学试卷(解析版) 题型:选择题
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.344L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入 6mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60mL B.40mL C.30mL D.15mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com