
���� ��2�����ݷ���ʽ2NO+O2=2NO2��2SO2+O2=2SO3��֪��������Ӧ��O2����ʱ������O2��Ӱ��ѹǿ���������������Ϊ������������һ�룬V��O2��=50mL���ݴ˿��ж���������ͨ��O2�����v��mL����Χ��
��2�����ݷ���ʽ2NO+O2=2NO2��2SO2+O2=2SO3��֪��Ҫʹ������ֻ��NO2��SO2�������壬����ʹNO����������ǡ����ȫ��Ӧ��������Ϊ������������һ�룻
��3������������ͨ��40ml O2��ſ�ʼ���ֺ���ɫ���Ҳ���ɫ��˵����ʱ�պð�SO3��Ӧ��ȫ������SO3��O2��2��1�Ĺ�ϵ��֪SO3��������������������һ�����������
��� �⣺��1�����ݷ���ʽ2NO+O2=2NO2��2SO2+O2=2SO3��֪��������Ӧ��O2����ʱ������O2��Ӱ��ѹǿ���������������Ϊ������������һ�룬V��O2��=50mL��
����ֻҪ����V��O2����50mL�����ڵ�ѹǿ�Ͳ��䣬
�ʴ�Ϊ������50mL��
��2�����ݷ���ʽ2NO+O2=2NO2��2SO2+O2=2SO3��֪��Ҫʹ������ֻ��NO2��SO2�������壬����ʹNO����������ǡ����ȫ��Ӧ���������������һ�룬V��O2��=50mL��
�ʴ�Ϊ��50��
��3������������ͨ��40ml O2��ſ�ʼ���ֺ���ɫ���Ҳ���ɫ��˵����ʱ�պð�SO3��Ӧ��ȫ�����ǵ�SO3��O2��2��1�Ĺ�ϵ��֪SO3Ϊ40mL��2=80mL��
��ԭ���������NO�����Ϊ��100mL-80mL=20mL��
�ʴ�Ϊ��20��
���� ���⿼���˻���ﷴӦ�ļ��㣬��ȷ������Ӧ��ʵ��Ϊ���ؼ���ע���������۷��ڻ�ѧ�����е�Ӧ�ã�����������ѧ���ķ�����������ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ����һ��Ҫ������ɫ�Լ�ƿ�У�������������ԭ���ǣ�4HNO3$\frac{\underline{\;���������\;}}{\;}$2NO2��+O2��+2H2O | |
| B�� | ����240mlŨ��Ϊ1 mol•L-1��NaOH��Һ���轫NaOH��������ձ��У���������ƽ��ȡ10.00g��ѡ��250ml������ƿ�������� | |
| C�� | �����¿������ʻ�������������Ũ���ᣬ����Ϊ�����¶��߲�������Ӧ | |
| D�� | ����ڼ���ʱ����ֽ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȳ���ʹ¯��˲��������ֲ��ܽ�ʡȼ�� | |
| B�� | �䲻��ʹ¯��˲������������Խ�ʡȼ�� | |
| C�� | ����ʹ¯��˲������ֿ��Խ�ʡȼ�� | |
| D�� | ���ܽ�ʡȼ�ϣ�����ʹ¯��˲����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
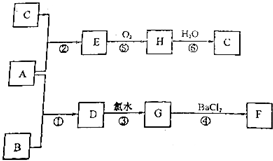
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
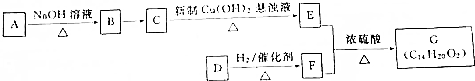
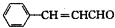 ��
��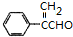 ��
��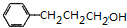 $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$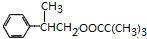 +H2O��CH3��3CCOOH+
+H2O��CH3��3CCOOH+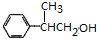 $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$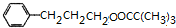 +H2O��
+H2O�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 39g���к���C�TC����Ϊ1.5NA | |
| B�� | 0.5molFeBr2���״����33.6L������Ӧʱת�Ƶ�����Ϊ3NA | |
| C�� | 1L0.5mol•L-1��NaClO��Һ�к��е�ClO-������Ϊ0.5NA | |
| D�� | ���³�ѹ�£�14g��C2H4��C3H6��ɵĻ�������к��е�ԭ������Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
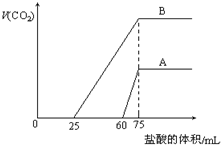 ȡ�����ݵ�Ũ�ȵ�NaOH��ҺA��B��ÿ��10mL���ֱ���A��B��ͨ�벻������CO2���ټ���������Һ����μ���0.2mol/L�����ᣬ��״���²�����CO2������������ӵ�������Һ���֮��Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
ȡ�����ݵ�Ũ�ȵ�NaOH��ҺA��B��ÿ��10mL���ֱ���A��B��ͨ�벻������CO2���ټ���������Һ����μ���0.2mol/L�����ᣬ��״���²�����CO2������������ӵ�������Һ���֮��Ĺ�ϵ��ͼ��ʾ���Իش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
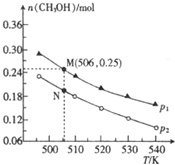 ����Ȼ��Ϊԭ�Ϻϳɼ״������ķ�����ˮú������Ŀǰ���ڿ�����ֱ����������
����Ȼ��Ϊԭ�Ϻϳɼ״������ķ�����ˮú������Ŀǰ���ڿ�����ֱ�����������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com