
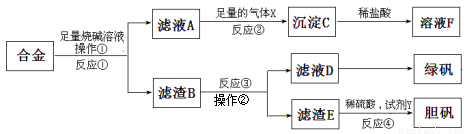
Ϊ̽����ҵ����������ͭ�Ͻ���ϵ������ã���ͬѧ��Ƶ�ʵ�鷽�����£�
��ش�
��1���̷��Ļ�ѧʽΪ ��
��2��д����Ӧ�ٵĻ�ѧ����ʽ ����Ӧ�����ɳ��������ӷ�Ӧ����ʽ ��
��3��Ϊ�˼����ҺD�к��еĽ������ӣ������ʵ�鷽��Ϊ���Լ���ѡ���� ��
��4��������B�еμ�ϡ����ʱ�����ַ�Ӧ���ʱ�һ������۷�ӦҪ�죬��ԭ���� ��
��5����������ɫ��ѧ���գ�������E�м���ϡ������Լ�Y�Ƶ������壬�Լ�YΪ��ɫҺ�壬��Ӧ�ܵ��ܻ�ѧ����ʽΪ ������������ɫ��ѧ���գ���ѡ�Լ�YΪ1mol/L�����ᣬ��ʹ3molCuȫ���ܽ�����Һ�к�ͭԪ�ص����ʽ�ΪCuSO4��������������� L��
��1��(2��) FeSO4��7H2O
��2����4�֣�2Al+2NaOH+2H2O=2NaAlO2+3H2�� AlO2-+CO2+2H2O=Al(OH)3��+HCO3-
(��2AlO2-+CO2+3H2O=2Al(OH)3��+CO32-) [δд���ӷ���ʽ��1�֣�����ƽ��1�֣����ӷ��Ŵ�0��]
��3��(3��) ���Թ�ȡ������ҺD��1�֣�������Һ�еμ�KSCN����NaSCN����NH4SCN)]
��Һ����������1�֣����ٵ�����ˮ����˫��ˮ����ͨ��Cl2�������Ѫ��ɫ������
Һ���д���Fe2+��1�֣���
��4����2�֣�ͭ������ϡ�����γ���ԭ��أ������˵绯��ʴ�����е���������
��5��(5��) Cu+H2O2+H2SO4=CuSO4+2H2O��2�֡���ƽ1�֣���ѧʽ��0�֣�
2��3�֣�[˵������ӦʽΪ3Cu+2HNO3+3H2SO4=3CuSO4++2NO��+4H2O]
��������
�����������1���̷�Ϊ�����������壬��ѧʽΪ��FeSO4��7H2O
��2����Ӧ��ΪAl��NaOH��Һ�ķ�Ӧ�����ӷ���ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2������Ӧ����ͨ�����������XΪCO2��CO2��H2O��AlO2-��Ӧ���ɵij���ΪAl(OH)3�����ӷ���ʽΪ��AlO2-+CO2+2H2O=Al(OH)3��+HCO3- (��2AlO2-+CO2+3H2O=2Al(OH)3��+CO32-)
��3����ҺD������ΪFeSO4������Fe2+��ԭ��Ϊ��Fe2+����ʹKSCN��ΪѪ��ɫ����������������Fe2+����ΪFe3+����Һ��ΪѪ��ɫ������ʵ�鷽��Ϊ�����Թ�ȡ������ҺD������Һ�еμ�KSCN����NaSCN����NH4SCN)]����Һ�����������ٵ�����ˮ����˫��ˮ����ͨ��Cl2�������Ѫ��ɫ������Һ���д���Fe2+��
��4������B�к�������ͭ�������μ�ϡ�����ͭ������ϡ�����γ���ԭ��أ�ʹ��Ӧ���ʼӿ졣
��5������EΪCu������ϡ������Լ�Y����CuSO4��������ɫ��ѧ���գ�YΪ��ɫҺ�壬���Լ�YΪH2O2����Ӧ�ܵ��ܻ�ѧ����ʽΪ��Cu+H2O2+H2SO4=CuSO4+2H2O��Cuȫ���ܽ�����Һ�к�ͭԪ�ص����ʽ�ΪCuSO4����ѧ����ʽΪ��3Cu+2HNO3+3H2SO4=3CuSO4++2NO��+4H2O��CuΪ3mol�������ĵ�HNO3Ϊ2mol�������������Ϊ��2mol��1mol?L?1=2L��
���㣺���⿼�黯ѧ���̵ķ�������ѧ����ʽ�����ӷ���ʽ����д�����ӵļ��顢ԭ���ԭ������ѧ���㡣


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�꽭��ʡ������У���ϵ��в��ԣ�һ����ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й����ʵ����ʺ����ʵ�Ӧ�þ���ȷ����
A��SO2���������ԣ�������Ư��ֽ��
B��̿���л�ԭ�ԣ�һ���������ܽ��������軹ԭΪ��
C��BaCO3��BaSO4��������ˮ��������������
D��Al2O3���кܸߵ��۵㣬���������������ռ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�꽭��ʡ�Ͼ��С��γ��и�����һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��������ʵ�Ӧ����ȷ����
A���Ȼ�����Һ�����ԣ������������������Ȼ�����Һ
B��̼������Һ�Լ��ԣ������ȵĴ�����Һ��ȥ����������������
C��������ѧ����ͨ�������ã��ɽ����ȵ�þ�ۿɷ��ڵ�������ȴ
D��ͭ�Ľ����Ա��������ɽ����ֽ�ˮ��������ͭ���Լ������帯ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��㶫ʡï���и����ڶ��θ߿�ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
��ҵ�����õ�����ࣨ��Ҫ����Fe2O3��CuO��Cr2O3�������������ʣ�����ͭ���Ƚ����������������£�
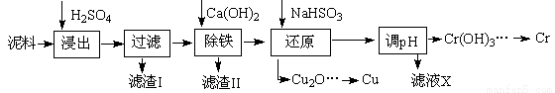
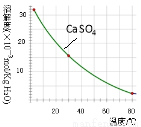
��֪�������ʳ�����pH��CaSO4���ܽ���������£�
| Fe3+ | Cu2+ | Cr3+ |
��ʼ����pH | 2��1 | 4��7 | 4��3 |
��ȫ����pH | 3��2 | 6��7 | a |
��1���ڽ��������г�������Fe2(SO4)3��Cr2(SO4)3��,��Ҫ����
��2���ڳ��������У���Ҫ��ȥFe3+��CaSO4,�������ز������ټ���ʯ�������pH�� ���ڽ���Һ���ȵ�80�棬 ��
��3��д����ԭ�����м���NaHSO3����Cu2O��������ӷ�Ӧ����ʽ ���˲����м���NaHSO3�õ�Cu2O�IJ���Ϊ95%����NaHSO3�����������˷��Լ��⣬������ֵ������� ��
��4��������Ũ�ȡ�1��10��5 mol?L-1��Ϊ������ȫ����ҪʹCr3+��ȫ������Ҫ����C(OH��)�� ����֪��Ksp[Cr(OH)3]=6��3��10-31��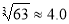 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��㶫ʡï���и����ڶ��θ߿�ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���г���I��II��ȷ�����������ϵ����
ѡ�� | ����I | ����II |
A | SO2����ˮ��Ư���� | ���߶���ʹ��ˮ��ɫ |
B | �õ���-KI����FeCl2 | Fe2+�������� |
C | ����Ͱ�ˮ���ܽ�Al(OH)3 | Al(OH)3�������������� |
D | CuSO4����������Ӿ�������� | ͭ����ʹ�����ʱ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��㶫ʡ�����и�������һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���н�����ʵ�Ļ�ѧ����ʽ�����ӷ���ʽ������ȷ����
A����ҵ�Ͽ��õ�ⷨ�Ʊ�Mg��MgCl2(����) 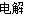 Mg + Cl2��
Mg + Cl2��
B����Ca(ClO)2��Һ��ͨ������CO2��Ca2++2ClO����H2O��CO2=2HClO��CaCO3��
C����CaSO4�����μ�أ�CaSO4(s) + Na2CO3(aq) CaCO3(s) + Na2SO4(aq)
CaCO3(s) + Na2SO4(aq)
D����FeSO4��ȥ���Է�ˮ�е�Cr2O72-��Cr2O72- + Fe2+ + 14H+ == 2Cr3+ + Fe3+ + 7H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��㶫ʡ�����и����ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
����ع㷺Ӧ���ڻ�϶�������ϵͳ���缫������Ni(OH)2��̼�ۡ���������Ϳ�����������Ƴɡ����ڵ��ʹ�ú�缫���϶Ի�����Σ����ij��ȤС��Ըõ�ص缫���Ͻ�����Դ�����о������ʵ���������£�
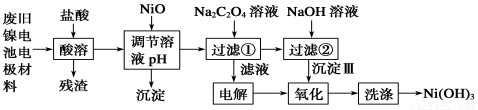
��֪����NiCl2������ˮ��Fe3����������Ni2������K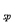 (Ni(OH)
(Ni(OH) ): 5.0��10-16 �� K
): 5.0��10-16 �� K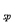 (NiC2O4): 4.0��10-10
(NiC2O4): 4.0��10-10
�ش��������⣺
��1�����ܺ�������������Ҫ�ɷ� �����������ƣ���
��2����NiO������Һ��pH�����������ijɷ�Ϊ____________________(�ѧʽ)����pH��ֽ�ⶨij��ҺpH�ľ�������� ��
��3��д������Na2C2O4��Һ��Ӧ�Ļ�ѧ����ʽ_____________________________��
��4��д������NaOH��Һ��������Ӧ�����ӷ���ʽ ���÷�Ӧ��ƽ�ⳣ��Ϊ ��
��5��������ɱ�������ò���֮һ ���ѧʽ����������Ni(OH)3 �����ϴ��Ni(OH)3 ������
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��㶫ʡ��Զ�и���4��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
þ����������ȼ�ϵ�ؾ��б������ߡ���ȫ������ŵ㣬�õ����Ҫ����ԭ����ͼ��ʾ����������ӦΪ��ClO�� + H2O + 2e�� = Cl�� + 2OH�������ڸõ�ص�������ȷ����
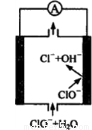
A���õ����þΪ������������ԭ��Ӧ
B����ع���ʱ��OH���������ƶ�
C����ع���ʱ��������Χ��Һ��pH�����ϱ�С
D���õ�ص��ܷ�ӦΪ��Mg + ClO�� + H2O = Mg(OH)2��+ Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��㶫ʡ�����з�خ���߿�ͳ����һ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ����٤����������ֵ������˵����ȷ���ǣ�������
A�����³�ѹ�£�1.7gH2O2�к��еĵ�����Ϊ0.9NA
B��1 mol.L-1CuCl2��Һ����2NA��Cl-
C��1 mol Na ������ O2��Ӧ������Na2O��Na2O2�Ļ�����ʧȥ2NA������
D����״���£�2.24L��������������Ϊ0.1NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com