
一种直接肼燃料电池的结构如图所示,下列说法正确的是
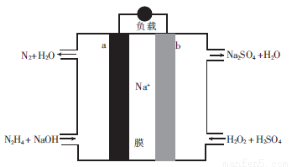
A.a极为电池的正极
B.电路中每转移6.02×1023个电子,则有1molNa+穿过膜向正极移动
C.b极的电极反应式为H2O2+2e-=2OH-
D.用该电池电解饱和食盐水,当阳极生成2.24L(标准状况)Cl2时,消耗肼0.1mol
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源:2015-2016学年宁夏六盘山中学高二上第二次月考化学试卷(解析版) 题型:选择题
氨水中所含有的分子和离子有①NH4+ ②H2O ③NH3 ④NH3·H2O ⑤H+ ⑥OH-
A.①②③ B.②③④⑤ C.②③④⑤⑥ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016届贵州市高三上学期第四次月考理综化学试卷(解析版) 题型:推断题
Ⅰ.A、B、C、D、E、X是中学常见的无机物,存在下图所示转化关系(部分生成物和反应条件略去),已知A由短周期非金属元素组成,B具有漂白性且光照易分解。
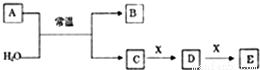
(1)若A为单质,且常温下0.1mol•L-1C溶液的pH为1,请回答以下问题:
①组成单质A的元素在元素周期表中的位置为______________________;
②A与H2O反应的离子反应方程式为______________________;
③X可能为________(填代号)。a.NaOH b.AlCl3 c.Na2CO3 d.NaAlO2
(2)若A为两种元素形成的化合物,且E与水反应生成G的浓溶液遇C有白烟产生则:
①A的电子式为______________________;
②A与H2O反应的化学反应方程式为______________________;
Ⅱ.某化合物A是一种易溶于水的不含结晶水盐,溶于水后完全电离出三种中学化学常见离子,其中有两种是10电子的阳离子。用A进行如下实验:取2.370gA溶于蒸馏水配成溶液;向该溶液中逐滴加入一定量的氢氧化钠溶液,过程中先观察到产生白色沉淀B,后产生能使湿润红色石蕊试纸变蓝的气体 C,气体不再产生时沉淀开始溶解,当沉淀恰好完全溶解时共用去氢氧化钠的物质的量为0.050mol.回答下列问题:
(1)请画出沉淀B中金属元素的原子结构示意图______________________;
(2)请写出沉淀B溶解在氢氧化钠溶液中的离子方程式______________________;
(3)请写出气体C与氯气发生氧化还原反应的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期12月模拟化学试卷(解析版) 题型:选择题
下列关于物质分类的组合正确的是
分类 | 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 |
A | 重水 | 氨水 | 氯化钾 | 碳酸钙 | 二氧化碳 |
B | 冰醋酸 | 漂白粉 | 硫酸钡 | 氟化氢 | 氨气 |
C | 胆矾 | 水泥 | 苛性钠 | 亚硫酸 | 石灰石 |
D | 氯化氢 | 分馏汽油 | 硝酸 | 醋酸 | 氯气 |
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上学期12月月考化学试卷(解析版) 题型:填空题
汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为什么2NO+2CO 2CO2+N2。在密闭容器中发生该反应时,随温度(T)和时间(t)的变化曲线如图所示。
2CO2+N2。在密闭容器中发生该反应时,随温度(T)和时间(t)的变化曲线如图所示。
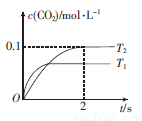
①T1_________(填“>”“<”或“=”)T2。
②在T2温度下,0~2s内的平均反应速率v(N2)=____________________。
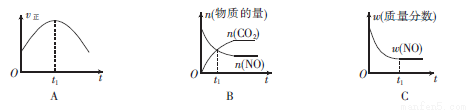
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________________。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用广泛的烟气氮氧化物脱除技术。用Fe作催化剂时,在氨气足量的情况下,不同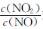 对应的脱氮率如图所示。
对应的脱氮率如图所示。
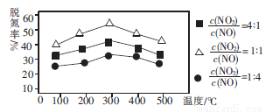
脱氮效果最佳的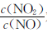 =________。此时对应的脱氮反应的化学方程式为_______________。
=________。此时对应的脱氮反应的化学方程式为_______________。
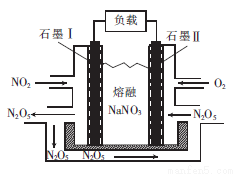
(3)NO2、O2和熔融NaNO3可形成燃料电池,其原理如图所示。该电池在使用过程中石墨I电极上生成N2 O5,其电极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上学期12月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值。下列说法正确的是
A.常温常压下,1.7gNH3所含的电子数为0.8NA
B.标准状况下,11.2LSO3所含的氧原子数为1.5NA
C.1molSiO2中含有Si—O键的数目为2NA
D.1molFe与足量的稀硝酸反应,转移的电子总数为3NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市四校高一上学期期中联考化学试卷(解析版) 题型:填空题
、高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子,制取高铁酸钠的化学方程式如下:
2Fe(NO3)3+16NaOH+3Cl2 = 2Na2FeO4+6NaNO3+6NaCl+8H2O
(1)标出该反应中电子转移的方向和数目。
(2)在上述反应中 (填元素名称)元素被氧化,氧化剂是 (填化学式)。
(3)当有2.408×1024 个电子发生转移时,参加反应的氯气在标准状况下的体积为 。
(4)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂。在水处理过程中,Na2FeO4中的铁元素转化为Fe(OH)3胶体,使水中悬浮物聚沉,Fe(OH)3胶体中分散质粒子直径的范围是  ,向Fe(OH)3胶体中逐滴加入HCl稀溶液至过量,会出现的现象是: .
,向Fe(OH)3胶体中逐滴加入HCl稀溶液至过量,会出现的现象是: .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北邯郸魏县一中、曲周县一中高一上期中化学试卷(解析版) 题型:选择题
下列离子检验的方法正确的是
A.某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl﹣
B.某溶液中加BaCl2溶液生成白色沉淀,说明原溶液中有SO42﹣
C.某溶液中加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+
D.某溶液中加稀硫酸溶液生成无色气体,说明原溶液中有CO32﹣
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高一上学期期中考试化学试卷(解析版) 题型:选择题
 设NA代表阿伏加德罗常数,下列说法中,正确的是
设NA代表阿伏加德罗常数,下列说法中,正确的是
A.2.3g金属钠全部变成钠离子时失去的电子数目为0.2NA
B.2g氢气所含的原子数目为NA
C.17gNH3所含的电子数为10NA
D.NA个氧分子和NA个氢分子的质量比等于16∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com