
| A. | 向MgCl2溶液中加入过量的NaOH溶液,Mg2+沉淀完全,则溶液中不含Mg2+ | |
| B. | Ksp小的物质其溶解能力一定比Ksp大的物质的溶解能力小 | |
| C. | 25℃时,由于Kw(ZnS)>Kw(CuS),所以ZnS在一定条件下可转化为CuS | |
| D. | 0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
分析 A.氢氧化镁在溶液中存在溶解平衡;
B.对于不同类型的难溶物,不能直接根据溶度积判断其溶解度大小;
C.从难溶电解质的转化的角度分析;
D.碘化银比氯化银更难溶,则溶液中氯离子浓度大于碘离子.
解答 解:A.向MgCl2溶液中加入过量的NaOH溶液,反应生成氢氧化镁沉淀,由于氢氧化镁在溶液中存在溶解平衡,则Mg2+沉淀完全时溶液中仍然含有Mg2+,故A错误;
B.当难溶物类型不同时,不能直接根据溶度积数据大小判断溶解度,则Ksp小的物质其溶解能力不一定比Ksp大的物质的溶解能力小,故B错误;
C.化学反应可向Ksp小的方向进行,因Ksp(ZnS)>Ksp(CuS),ZnS浊液中加入硫酸铜溶液,可转化为CuS沉淀,故C正确;
D.0.1molAgCl和0.1molAgI混合后加入0.1L水中,氯化银的溶解度大于碘化银,则所得溶液的c(Cl-)>c(I-),故D错误;
故选C.
点评 本题考查了离子浓度大小比较、难溶物溶解平衡及其应用,题目难度中等,明确难溶物溶解平衡及其影响为解答关键,注意掌握溶度积与溶解度之间的关系,试题培养了学生的分析能力及灵活应用能力.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物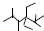 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 用酸性KMnO4 溶液可鉴别2-丁烯和正丁醛 | |
| C. | 用甘氨酸[H2N-CH2-COOH]和丙氨酸[CH3CH(NH2)COOH]缩合最多可形成3 种二肽 | |
| D. | 乙醇、乙二醇、丙三醇的沸点依次升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物XW中含有共价键 | |
| B. | 化合物ZW中含有离子键 | |
| C. | X和Z可以形成离子化合物ZX | |
| D. | 化合物ZYX和ZYW所含有的键型不一样 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
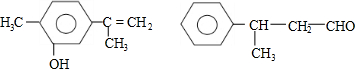
| A. | 可用红外光谱区分,但不能用核磁共振氢谱区分 | |
| B. | 分子中最多都有10个碳原子共平面 | |
| C. | 不是同分异构体 | |
| D. | 均能与溴水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
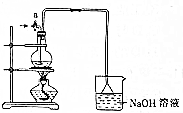 某化学探究小组为探究能与碳反应的浓硫酸的最低浓度,设计了如图实验装置进行实验.
某化学探究小组为探究能与碳反应的浓硫酸的最低浓度,设计了如图实验装置进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
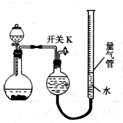 某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:| 实验 | 药品 | 制取气体 | 量气管中液体 |
| Ⅰ | Cu、稀HNO3 | NO | H2O |
| Ⅱ | NaOH(s)、浓氨水 | NH3 | |
| Ⅲ | 过氧化钠、水 | O2 | H2O |
| Ⅳ | 镁铝合金、NaOH溶液 | H2 | H2O |

| 编号 | 镁铝合金 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 346.3mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 345.7mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
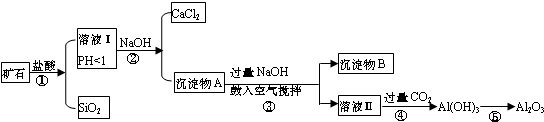
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m+n<p | B. | 平衡向逆反应方向移动 | ||
| C. | C的体积分数增大 | D. | A的转化率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③⑤ | C. | ①④⑤ | D. | ②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com