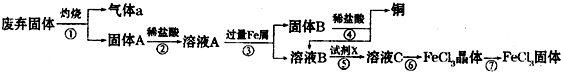
(2012?东城区模拟)牙膏是由摩擦剂和一些可溶于水的物质组成.常用的摩擦剂主要有:CaCO
3、Al(OH)
3、SiO
2?nH
2O、Ca
3(PO
4)
2.资料显示:Ca
3(PO
4)
2高温不分解;Ca
3(PO
4)
2和CaHPO
4不溶于水;Ca(H
2PO
4)
2溶于水;Ca
3(PO
4)
2+4H
+=3Ca
2++2H
2PO
4-.
(1)为测定某牙膏的酸碱性和摩擦剂的主要成分,甲同学设计并完成以下实验:
①取一小段牙膏与一定量蒸馏水充分搅拌后过滤,用pH试纸测定滤液酸碱性的方法是
用干燥洁净的玻璃棒蘸滤液,滴在pH试纸上,经与标准比色卡比较后
用干燥洁净的玻璃棒蘸滤液,滴在pH试纸上,经与标准比色卡比较后
(填相应操作),读出其pH接近8;
②若向①所得不溶物中加入适量稀盐酸,得到澄清溶液,有气体产生,则产生气体的离子方程式是
CaCO3+2H+=Ca2++CO2↑+H2O
CaCO3+2H+=Ca2++CO2↑+H2O
;若向①所得不溶物中加入NaOH溶液,经测定,不溶物的质量不发生变化;
③取②中加稀盐酸后所得溶液,加入过量NaOH溶液,观察到最终有沉淀生成,生成该沉淀的离子方程式是
2H2PO4-+3Ca2++4OH-=Ca3(PO4)2+4H2O
2H2PO4-+3Ca2++4OH-=Ca3(PO4)2+4H2O
;根据上述实验,摩擦剂中一定含有的物质是
CaCO3、Ca3(PO4)2
CaCO3、Ca3(PO4)2
.
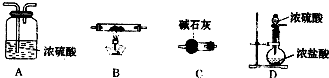
(2)乙同学用如下装置(已检验气密性,夹持装置略)通过测CO
2的质量来计算牙膏不溶物中CaCO
3的含量.

①滴加稀盐酸之前的部分操作:…打开弹簧夹,通入N
2一段时间;再将盛有碱石灰的干燥管连接在整套装置上….按此顺序进行操作的原因是
避免碱石灰吸收装置中原有空气中的CO2
避免碱石灰吸收装置中原有空气中的CO2
;
②用上述装置重复几次实验,所测样品中CaCO
3的含量均偏高,若实验过程中的操作没有失误,分析可能的原因是
干燥管中的碱石灰吸收空气中的CO2或H2O
干燥管中的碱石灰吸收空气中的CO2或H2O
或
NaHCO3溶液除HCl时产生了CO2
NaHCO3溶液除HCl时产生了CO2
;
③设计实验不用其他任何试剂(仪器可任选),仅用牙膏不溶物样品测定摩擦剂中CaCO
3含量的方法是
称量不溶物样品在高温下完全分解前后的质量
称量不溶物样品在高温下完全分解前后的质量
(不必填具体操作).