
分析 (1)硫酸铁为强电解质,完全电离出铁离子和硫酸根离子;碳酸氢钠为强电解质,完全电离生成钠离子和碳酸氢根离子;
(2)盐酸与碳酸钙反应生成氯化钙和水;
氢氧化钡与硫酸反应生成硫酸钡和水;
(3)H++OH-═H2O课表上盐酸与氢氧化钠反应;
CO32-+2H+═CO2↑+H2O可以表示碳酸钠与盐酸反应;
(4)氯化钙能与碳酸钠反应生成碳酸钙沉淀,氯化钠与氯化钙不反应;
(5)铝能够与氢氧化钠反应生成可溶性偏铝酸钠而溶解,铁与氢氧化钠不反应,过滤即可除去铝.
解答 解:(1)硫酸铁为强电解质,完全电离出铁离子和硫酸根离子,电离方程式:Fe2(SO4)3=2Fe3++3SO42-;碳酸氢钠为强电解质,完全电离生成钠离子和碳酸氢根离子,电离方程式:NaHCO3=Na++HCO3-;
故答案为:Fe2(SO4)3=2Fe3++3SO42-;NaHCO3=Na++HCO3-;
(2)盐酸与碳酸钙反应生成氯化钙和水,离子方程式:CaCO3+2H+=Ca2++CO2↑+H2O,氢氧化钡与硫酸反应生成硫酸钡和水,离子反应为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;
(3)H++OH-═H2O课表上盐酸与氢氧化钠反应,化学方程式:HCl+NaOH=NaCl+H2O;
CO32-+2H+═CO2↑+H2O可以表示碳酸钠与盐酸反应,化学方程式:Na2CO3+2HCl═CO2↑+H2O+2NaCl;
故答案为:HCl+NaOH=NaCl+H2O;Na2CO3+2HCl═CO2↑+H2O+2NaCl;
(4)氯化钙能与碳酸钠反应生成碳酸钙沉淀,反应离子方程式:Ca2++CO32-=CaCO3↓,氯化钠与氯化钙不反应,所以可以用氯化钙检验氯化钠和碳酸钠;
故答案为:氯化钙溶液;Ca2++CO32-=CaCO3↓;
(5)铝能够与氢氧化钠反应生成可溶性偏铝酸钠而溶解,离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑,铁与氢氧化钠不反应,过滤即可除去铝;
故答案为:氢氧化钠溶液;2Al+2OH-+2H2O═2AlO2-+3H2↑.
点评 本题为综合题,考查了电解质电离方程式书写,离子反应方程式书写,物质的检验、物质的鉴别和除杂,熟悉物质的性质及发生反应的实质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | SO2可以使溴水褪色,所以SO2具有漂白性 | |
| B. | 因为氢氧化铁胶体具有吸附性,所以常用于净水 | |
| C. | 因为液态HCl不导电,所以HCl是非电解质 | |
| D. | NH3的水溶液可以导电,所以NH3是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸用量偏大,生成CO2气体的量偏大 | |
| B. | 盐酸用量偏大,生成CO2气体的量偏小 | |
| C. | 盐酸用量偏小,生成CO2气体的量偏大 | |
| D. | 盐酸用量偏小,生成CO2气体的量偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有A、B、C、D、E是前四期的元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子有3能级,且有3个未成对电子;D的最外层电子数是内层电子数的3倍.基态的E是前四周期中未成对电子数最多的原子.
有A、B、C、D、E是前四期的元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子有3能级,且有3个未成对电子;D的最外层电子数是内层电子数的3倍.基态的E是前四周期中未成对电子数最多的原子.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.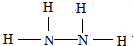 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH(CH2Br)2 | B. | (CH3)2BrCH2Br | C. | C2H5CHBrCH2Br | D. | CH3(CHBr)2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
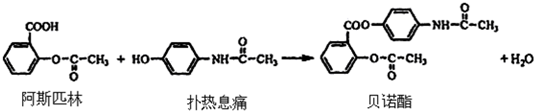
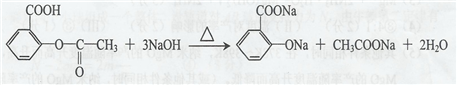 .
.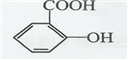 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+,草酸被氧化成CO2.某课题组研究发现,少量铁明矾[Al2Fe(SO4)4•24H2O]即可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+,草酸被氧化成CO2.某课题组研究发现,少量铁明矾[Al2Fe(SO4)4•24H2O]即可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:| 实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 | 10 | 30 |
| ③ | 5 | 60 | V1 | 20 |
| 实验方案 | 预期实验结果和结论 |
| 用等物质的量的K2SO4•Al2(SO4)3•24H2O代替实验①中的铁明矾,控制其他条件与实验①相同,进行对比实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C3H6Cl2的同分异构体有3种 | |
| B. | 分子式为C5H12O,且能与金属钠反应的同分异构体有8种 | |
| C. | 分子式为C4H8O2属于羧酸类的同分异构体有2种 | |
| D. | 分子式为C4H8O2属于酯类的同分异构体有4种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com