
| A. | 1mol铜片与含2molH2SO4的浓硫酸共热 | |
| B. | 1molMnO2粉末与含2molH2O2的溶液共热 | |
| C. | 常温下1mol铝片投入足量的浓硫酸中 | |
| D. | 常温下1mol铜片投入含4molHNO3的浓硝酸中 |
分析 A.金属铜和稀硫酸不反应,只能和浓硫酸反应;
B.反应中二氧化锰为催化剂,反应前后二氧化锰的量不变;
C.常温下,金属铝遇到浓硫酸发生钝化;
D.金属铜和浓硝酸以及稀硝酸均会发生反应.
解答 解:A.根据反应方程式可知64g即1mol铜片与含2 molH2SO4浓硫酸共热恰好反应,但是实际上随着反应的进行,浓硫酸会变稀,金属铜和稀硫酸不反应,所以金属铜会剩余,故A错误;
B.二氧化锰在反应中作催化剂,所以二氧化锰不会溶解,故C错误;
C.常温下,金属铝遇到浓硫酸发生钝化,所以常温下1 mol铝片投入足量的浓硫酸中金属会剩余,故C错误;
D.金属铜和浓硝酸以及稀硝酸均会发生反应,1mol铜片投入含4mol的浓硝酸中,会恰好反应,故D正确;
故选D.
点评 本题考查了常见元素单质及其化合物性质,题目难度不大,明确常见金属单质与酸的反应情况为解答关键,A为易错点,注意浓硫酸变成稀硫酸后反应停止,试题培养了学生的灵活应用能力.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:解答题
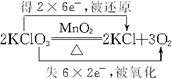 .
.
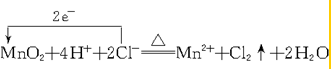 .
.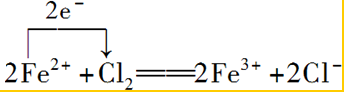 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6、C2H4O | B. | C2H4O、C2H4O2 | C. | C2H6O、C3H6O3 | D. | C3H8O3、C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CHCl-CHO | B. | CH3-CHBr-CHBr-CH3 | ||
| C. | CH3-C≡C-CHO | D. | 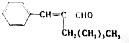 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑩ | ⑥ | |||||
| 3 | ① | ③ | ④ | ⑧ | ⑨ | ⑦ | ||
| 4 | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积减半,则N2O4的浓度为原来的两倍 | |
| B. | 平衡向右移动,混合气体的颜色一定会变浅 | |
| C. | 体积减半,压强增大,但小于原来的2倍 | |
| D. | 平衡向右移动,但混合气体密度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com