
反应2SO2+O22SO3达到平衡状态后,下列说法正确的是( )
A.三氧化硫的生成速率与分解速率相等
B.二氧化硫、氧气、三氧化硫的分子数之比是2:1:2
C.二氧化硫与氧气不再化合生成三氧化硫
D.降低温度,原化学平衡状态未被破坏
科目:高中化学 来源: 题型:
下列各组试剂(括号内的是滴加试剂)做溶液导电性实验的过程中,可以观察到灯泡由亮变暗直至熄灭,然后又逐渐变亮的是( )
|
| A. | BaCl2溶液(稀硫酸) | B. | 氨水(醋酸溶液) |
|
| C. | Ba(OH)2溶液[Ba(HCO3)2溶液] | D. | Ba(OH)2溶液(NaHSO4溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:
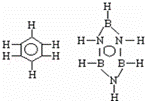
已知化合物B3N3H6(硼氮苯)与苯的分子结构相似,如图所示,则硼氮苯的四氯取代物(B3N3H2Cl4)的同分异构体的数目为( )
|
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
不同温度(T1和T2)时,硫酸钡在水中的沉淀溶解平衡曲线如图所示,已知硫酸钡在水中溶解时吸收热量。下列说法正确的是

A. T1>T2 B. 加入BaCl2固体,可使a点变成c点
C. c点时,在T1、T2两个温度下均有固体析出 D. a点和b点的Ksp相等
查看答案和解析>>
科目:高中化学 来源: 题型:
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用煤矸石的工艺流程如下图所示。
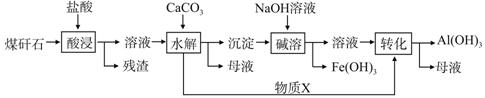
(1)写出“酸浸”过程中主要反应的离子方程式(任写一个):
。
(2)物质X的化学式为________。“碱溶”时反应的离子方程式为__________________。
(3)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得Al(OH)3产品,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续的操作过程是 ,再加入CaCO3调节pH到5.4,过滤得到Al(OH)3
(4)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向AlCl3饱和溶液中不断通入HCl气体,可析出大量AlCl3·6H2O晶体。结合化学平衡移动原理解释析出晶体的原因:
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个固定容积为2 L的密闭容器中2 mol A和1 mol B发生反应2A(g)+B(g)3C(g)+D(g),达到平衡时,C的浓度为0.3 mol/L,则A的浓度和B的浓度分别是( )
A.0.2 mol·L-1 0.1 mol·L-1
B.0.4 mol·L-1 0.2 mol·L-1
C.0.8 mol·L-1 0.4 mol·L-1
D.0.6 mol·L-1 0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应:2NO2(g)2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是( )
①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为221的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的压强不再改变的状态 ⑦混合气体的平均摩尔质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦
C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离平衡曲线如图所示:

A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡到达B点。
(1)25℃时水的离子积为________________,100℃时水的离子积为________________。
(2)100℃时,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,正确的是( )
|
| A. | 碳酸氢钙溶液与足量盐酸反应Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑ |
|
| B. | 稀盐酸和碳酸钙反应 CO32﹣+2H+=CO2↑+H2O |
|
| C. | 碳酸钠溶液与醋酸反应 CO32﹣+2H+=CO2↑+H2O |
|
| D. | 大理石溶于醋酸的反应 CaCO3+2CH3COOH=Ca2++2CH3COO﹣+CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com