
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2 (s)+Mn2O3(s),下列说法错误的是( )
(s)+Mn2O3(s),下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池正极反应为2MnO2(s)+H2O(l)+2e-―→Mn2O3(s)+2OH-(aq)
C.电池工作时,负极附近溶液碱性增强
D.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g
科目:高中化学 来源: 题型:
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。
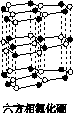
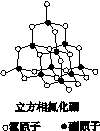
(1)基态硼原子的电子排布式为________。
(2)关于这两种晶体的说法,正确的是________(填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B—N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为________,其结构与石墨相似却不导电,原因是_____________________________________________________。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为________。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根椐这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是________________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4 含有________mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海藻中提取碘的流程图如下:
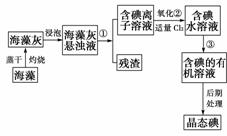
(1)指出提取碘的过程中有关的实验操作名称:
①________________,③________________。
写出过程②中有关反应的离子方程式:____________________________________________。
(2)提取碘的过程中,可供选择的有机溶剂是________(填序号)。
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是________。
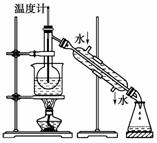
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出上图所示实验装置中的错误之处:
①________________________________________________;
②________________________________________________;
③________________________________________________。
(5)进行上述蒸馏操作时,使用水浴的原因是____________,最后晶体碘在________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材 料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是( )
料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是( )
A.水既是氧化剂又是溶剂
B.放电时正极上有氢气生成
C.放电时OH-向正极移动
D.总反应为:2Li +2H2O===2LiOH+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O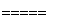 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是________。
(2)放电时,正极发生________(填“氧化”或“还原”)
反应;已知负极反应为Zn-2e-+2OH-===Zn(OH)2,则正极反应为________________________________________________________________________。
(3)放电时,________(填“正”或“负”)极附近溶液的碱性增强。
查看答案和解析>>
科目:高中化学 来源: 题型:
三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,再加入适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法不正确的是
A.可用铁作阳极材料
B.电解过程中阳极附近溶液的pH降低
C.阳极反应方程式为:2Cl--2e-=Cl2
D.1 mol二价镍全部转化为三价镍时,外电路中通过了1 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
在水溶液中能大量共存的离子组是 ( )
A.K+ 、Al3+ 、SO42-、OH- B.Ca2+ 、Na+、Cl-、NO3-
C.Na+ 、NH4+ 、NO3-、OH- D.Na+ 、H+ 、CO32-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com