
����Ŀ����2L���ܱ������У��������»�ѧ��Ӧ��CO2��g����H2��g��![]() CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 600 | 800 | 830 | 1000 | 1200 |
K | 0.25 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK �� ��
��2���÷�ӦΪ ��Ӧ��ѡ��������������������������Ӧ��ƽ�������ͨ��һ����CO2����ƽ�ⳣ��K��________��CO2��ת����________��(����������������С������������)
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬�������� ����ѡ�۷֣���
a��������ѹǿ���� b�����������c(CO)���� c��v��(H2)��v��(H2O) d��c(CO2)��c(CO)
��4���� 600��ʱ���������г���1mol CO��1mol H2O����Ӧ�ﵽƽ���CO��ת������ ��
���𰸡���1��![]() ��2������ ���� ��С ��3��bc ��4��
��2������ ���� ��С ��3��bc ��4��![]()
��������
��1��ƽ�ⳣ������������Ũ�ȵ���֮���뷴Ӧ��Ũ����֮����֮�ȣ���K ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��2���ӱ�����Կ��������¶ȵ����ߣ�ƽ�ⳣ�������¶�����ƽ���������ƶ�����ӦΪ���ȷ�Ӧ��ƽ�ⳣ��ֻ���¶��йأ��¶Ȳ���ƽ�ⳣ�����䣬�ʷ�Ӧ��ƽ�����ͨ��һ����CO2ƽ�ⳣ�����䣬ͨ��һ����CO2��H2��ת���ʻ���ߣ���CO2��ת���ʻ��С���ʴ�Ϊ�����ȣ����䣻��С��
��3����Ӧ�������������ķ�Ӧ����ϵ��ѹǿһֱ���ֲ��䣬�ʲ�����ѹǿ���ж��Ƿ�ﵽƽ��״̬��
a���÷�Ӧ��һ�������������ķ�Ӧ�������Ƿ�ﵽƽ�⣬ѹǿʼ�ղ��䣬�ʴ���
b�����ʵ�Ũ�Ȳ�����ƽ��״̬�ı�־����c(CO)���䷴Ӧ�ﵽ��ƽ�⣬����ȷ��
c������v��(H2)��v��(H2O) �� v��(H2)��v��(H2O) ��v��(H2O)= v��(H2O)��ͬ�����ʵ��������ʺ�����������ȣ���Ӧ�ﵽ��ƽ�⣬����ȷ��
d��c(CO2)��c(CO)������˵��Ũ�Ȳ��ٱ仯���ʴ���
bc��ȷ���ʴ�Ϊ��bc��
��4����Ӧ�������ı䣬�µ�ƽ�ⳣ��Ϊԭ���ĵ�����K���£�=1/0.25=4,��CO��Ӧ��x mo1/L�������⽨����������ʽ��
CO��g����H2O��g��![]() CO2��g����H2��g��
CO2��g����H2��g��
C��ʼ(mo1/L) 0.5 0.5 0 0
C�仯(mo1/L) x x x x
Cƽ��(mo1/L) 0.5-x 0.5-x x x
�ɻ�ѧƽ�ⳣ��K=![]() =
=![]() =4�����x=
=4�����x=![]() mo1/L���ʴ�Ϊ
mo1/L���ʴ�Ϊ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɫ����A����������Ͷ�뵽��ɫ��ҺB�з�����ͼת����ϵ��

(1)�ɴ˿����ƶϣ�AΪ________(�ѧʽ����ͬ)��BΪ_______��XΪ_______��CΪ_________��EΪ_________��
(2)д��A��B��Ӧ�Ļ�ѧ����ʽ�� ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ʒӵ�һ�ֺϳ�·����ͼ��

����˵������ȷ���ǣ� ��
A.������X������ˮ
B.��NaOHˮ��Һ�м��ȣ�������X�ɷ���ȡ����Ӧ
C.��һ��������������Y����CH3COOH�������۷�Ӧ
D.��FeCl3��Һ�ɼ�����X��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�ƽԭ��������ˮ����������̺����ϸߣ�����д������ܴﵽ����ˮ��������ˮ�����̵���Դ��Ҫ�ǿ���FeCO3��MnCO3��
(1)�����������ˮ�����������ߣ���ϻ�ѧ�����ƽ���ƶ��ǶȽ���ԭ��_______��
(2)ȥ��Fe2+
�ٳ����˳ؾ�������3��7������ϱ����γ�______ɫ���ʣ���ɷ���Fe(OH)3��ʹ����Һ��Fe2+����Ѹ���½��������ù�����ͼ��ʾ��
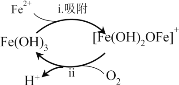
�ڽ�����ii�����ӷ���ʽ����������________��
����i��Fe2++Fe(OH)3=[Fe(OH)2OFe]++H+
����ii��4[Fe(OH)2OFe]++ +10H2O= +
����������߹���ii��Ӧ���ʵĴ�ʩ��______(�����)��
A. �����¶� B. ͨ������O2 C. ����
(3)ȥ��Mn2+
������˳��м���ClO2��Mn2+����ΪMnO2�����ŷ�Ӧ���У��˳���Һ��pH___(�������������С������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᣨ�Ҷ��ᣩ��������Ȼ���ֲ���У���������κͼ���������ˮ���������Ϊ���������ᾧ��(H2C2O4��2H2O)��ɫ���۵�Ϊ101����������ˮ��������ˮ��������170�����Ϸֽ⡣���顢������λͬѧ�Բ���ֽ�������̽��������ͬѧ��Ϊ������ֽ��������CO2������ͬѧ��Ϊ������ֽ�����л���CO���ش��������⣺
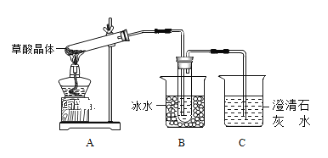
(1)����ͬѧ������ͼ��ʾ��װ�����ӣ�ͨ��ʵ�������ᾧ��ķֽ�������Aװ��ǰ��Ҫ���еIJ�����______________________��װ��C�пɹ۲쵽��������______________________________��װ��C�з����Ļ�ѧ����ʽ_________________���ɴ˿�֪���ᾧ��ֵIJ�������___________���ѧʽ����
(2)����ͬѧ��Ϊ���ᾧ��ֽ�IJ����к���CO��Ϊ������֤��ѡ�ü���ʵ���е�װ��A��B����ͼ��ʾ�IJ���װ�ã������ظ�ѡ�ã�����ʵ��.
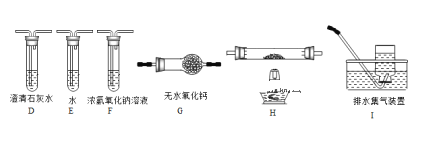
������ͬѧ��ʵ��װ���У��������ӵĺ���˳��ΪA��B��F��D��G____________��������˳��ȫװ�ã����д��ĸ����װ��H��Ӧ����ʢ�е�������______________���˷�Ӧ���з�����Ӧ�Ļ�ѧ����ʽ��_______________________��
����֤�����ᾧ��ֽ��������CO��������_____________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������Ȼ�ѧ����ʽ���ش�����������
2H2(g)+O2(g)![]() 2H2O��1�� ��H=571.6 kJ �� mol1
2H2O��1�� ��H=571.6 kJ �� mol1
C3H8(g)+5O2(g)![]() 3CO2(g)+4H2O(l) ��H=2 220 kJ �� mol1
3CO2(g)+4H2O(l) ��H=2 220 kJ �� mol1
��1��H2��ȼ����Ϊ_______��C3H8��ȼ����Ϊ_______��
��2��1 mol H2��2 mol C3H8��ɵĻ��������ȫȼ���ͷŵ�����Ϊ______________��
��3������H2��C3H8�Ļ�����干5 mol����ȫȼ��ʱ����3 847 kJ�����ڻ��������H2��C3H8���������_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɫ����A:�ٷ��ڿ����п��������ɰ�ɫ����B���ڽ�A��ȼ������ʻ�ɫ�����ɵ���ɫ����C����A��B��C��������ɫҺ��D��Ӧ�����ɼ�������E������A��D��Ӧʱ���������ɿ�ȼ������F��C��D��Ӧ��������һ������G����F��G��Ϻ�����ɾ��ҷ�Ӧ��������ը��������D���ݴ��ж�:
��1��A______��B______��C______��D________��E____��F_______��G_______�����ѧʽ��
��2��д���йط�Ӧ�Ļ�ѧ����ʽ:
��___________________________________________��
��__________________________________________��
��__________________________________________��
��__________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Դ������κ�����Ϊԭ���Ʊ�����K2FeO4�IJ����������£�
���Ʊ�NaClOǿ���Ա�����Һ��
�ٽ�20 mL NaOH��Һ��������b�У���ˮԡ��ȴ��ͨ��Cl2�����裬ֱ����Һ��Ϊ����ɫ����������ɫ��������Ϊֹ��װ������ͼ��ʾ����

�ڽ����ñ���NaClO�����ձ���������ˮԡ�У��ּ��μ���20 g NaOH���岢���Ͻ��裬���ˣ���NaClOǿ���Ա�����Һ��
(1)��װ����a�ܵ�������_____________________________________________��
(2)д����װ���з�Ӧ�Ļ�ѧ����ʽ_____________________________________��
(3)ʯ�����������___________________________________________________��
(4)��Ӧ����������ˮԡ��ȴ��ԭ����___________________________________��
�ϳ�K2FeO4��
�ٳ�ȡ5.05 g Fe(NO3)3��9H2O����Է�������Ϊ404�����壬����ˮԡ�з����������������Һ�������Ͻ��裬��Ӧ1Сʱ����Һ�����Ϻ�ɫ����Na2FeO4����
�����ķ����ȥNa2FeO4ˮ��õ���Fe(OH)3���壬���ϲ���Һ�����Ϻ�ɫ����
����ڵ��ϲ���Һ�л�������KOH������Һ50.00mL����ˮԡ����5 min�����ˣ���K2FeO4����Է�������Ϊ198���ֲ�Ʒ��
�ܽ��ֲ�Ʒ�ؽᾧ�����������ϴ�ӣ����º�ɣ��ô���Ʒ2.13 g��
(5)�ϳ�Na2FeO4�����ӷ���ʽΪ____________________________________��
(6)���̢ۼ��뱥��KOH��Һ���ɵõ�K2FeO4�ֲ�Ʒ��ԭ����__________��
(7)�������ϴ�ӵ�Ŀ����__________________________________________��
(8)K2FeO4�IJ���Ϊ___________��������0.1%����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com