
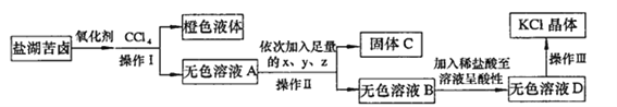
【题目】某研究性学习小组拟取苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等)来制取较纯净的氯化钾晶体及液溴,设计了如下流程:
回答以下问题:
(1)操作I的名称是__________________。从橙色液体中分离出溴,所采取的操作需要的主要玻璃仪器除酒精灯、温度计、锥形瓶外,还需要
_________________________。
(2)试剂z的化学式为_____________;检验SO42-已除尽的方法是_____________________________。
(3)无色溶液B中加入稀盐酸至溶液呈酸性,发生反应的离子方程式为___________________。
【答案】 萃取分液 蒸馏烧瓶、冷凝管、牛角管(接引管) K2CO3 取无色溶液D少许,加入BaCl2溶液,若没有白色沉淀,则SO42-已除尽 H++OH-=H2O、 2H++CO32-=H2O+CO2
【解析】(1)操作Ⅰ为互不相溶的液体的分离,应为萃取分液,从橙色液体中分离出溴,应为蒸馏操作,以此判断所需要的仪器;(2)除去溶液中的Mg2+、SO42-,应分别加入过量的BaCl2、KOH、K2CO3,检验SO42-已除尽,应加入BaCl2溶液,观察是否有沉淀生成;(3)无色溶液B中主要含有过量的氢氧化钾和碳酸钾。
(1)氧化剂应为氯气,通入氯气发生:Cl2+2Br-=2Cl-+Br2,加入CCl4,溴易溶于CCl4,溶液分层,用萃取、分液的方法分离;由于溴和CCl4的沸点不同,可用蒸馏的方法分离,蒸馏时用到的仪器有酒精灯、温度计、蒸馏烧瓶、冷凝管、牛角管、锥形瓶等;
(2)除去溶液中的Mg2+、SO42-,应分别加入过量的BaCl2、KOH、K2CO3,类似于粗盐的提纯,加入过量BaCl2可除去SO42-,加入过量KOH溶液可除去Mg2+,最后加入K2CO3可除去BaCl2,检验SO42-已除尽的方法是取无色溶液D,加入BaCl2溶液,若没有白色沉淀,则SO42-已除尽;(3)无色溶液B中主要含有过量的氢氧化钾和碳酸钾,故加入稀盐酸至溶液呈酸性,发生反应的离子方程式为H++OH-=H2O、 2H++CO32-=H2O+CO2。


科目:高中化学 来源: 题型:
【题目】完成以下四个小题:
(1)请完成下列各空:
① pH=a的CH3COOH溶液稀释100倍后所得溶液pH______a +2(填“>”或“<”)
② 0.01mol/LCH3COOH溶液的pH______2(填“>”、“<”或“==”);(用电离方程式表示其原因):_________________________________;
③ 0.1mol/LCH3COONa溶液的pH______7(填“>”或“<”),(用离子方程式表示其原因):______________________________;
(2)请你提出两种方案,证明HNO2酸是弱电解质:(只需简明写出方案,不需写出具体步骤,以下项目可不填满也可增加项目)
①___________________________________________________________________________
②_________________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】游泳池的水变绿主要是因为细菌及藻类的急剧繁殖导致的。
(1)含氯物质可以作为游泳池的消毒剂。一般水质正常的游泳池消毒后水中的余氯应保持在0.3~0.5 mg/L,pH保持在7.4~7.6,这个环境下细菌和藻类都不易生长和繁殖。
①夏季,露天游泳池水由于连续下雨会导致藻类大量繁殖,其原因是_____________________。
②消毒剂的错误使用也会导致藻类大量繁殖,游泳池水变绿。若水中的余氯以次氯酸形式存在,再加入H2O2进行消毒也会导致池水变绿,写出次氯酸与H2O2发生反应生成盐酸的化学方程式____________________。
(2)处理池水变绿的方法分为五步。
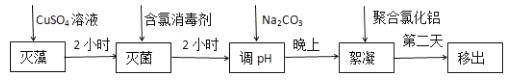
①灭藻原理是铜离子可以使叶绿体中毒无法光合作用而死亡,加入CuSO4溶液后需要打开水循环系统,其作用是__________________________。
②含氯消毒剂杀菌消毒主要体现出的化学性质是_________________。
③选用Na2CO3调节pH至7.5,用化学用语和文字解释其原因________________。
④ 聚合氯化铝可将悬浮物和被杀灭的细小藻类沉淀到池底,第二天将池底沉淀移出。稀释聚合氯化铝会产生胶体,其离子反应方程式是_____________________________;当温度大于80℃时,水体中铝离子的总浓度会降低,其原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锶(SrSO4)常用于烟火和陶瓷工业,可在Na2SO4溶液中加入锶盐溶液沉淀而得。下图表示不同温度下,SrSO4溶液中lg[c( Sr2+)]与lg[c( SO42-)]之间的关系。下列有关说法正确的是 ( )

A. 图像中a 、c两点的溶度积Ksp ( a ) < Ksp ( c )
B. 363K时Ksp (SrSO4) = 1.0×10ˉ3.2
C. SrSO4的溶解度随温度升高而增大
D. 313K时,b点对应的溶液为饱和溶液,d点对应的溶液为不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备。请回答下列有关问题:
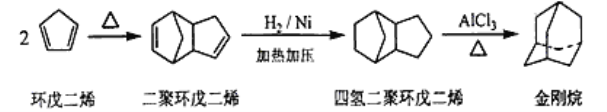
(1)环戊二烯分子中最多有____________个原子共平面。
(2)金刚烷的分子式为_________,其分子中的—CH2—基团有______个,金刚烷的一氯代物有______种。
(3)由环戊二烯生成二聚环戊二烯的反应类型是_______。
(4)已知烯烃能发生如下反应:![]() RCHO+R’CHO,请写出下列反应产物的结构简式:
RCHO+R’CHO,请写出下列反应产物的结构简式: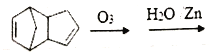 _________________,该产物中官能团的名称是___________________。
_________________,该产物中官能团的名称是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素原子的最外层只有2个电子,则该元素
A. 一定是IIA族元素 B. 一定是金属元素
C. 一定是正二价元素 D. 可能是金属元素,也可能不是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(16分)下图中的实验装置可用于制取乙炔。请填空:

(1)图中,A管的作用是 。
制取乙炔的化学方程式是 。
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 ,乙炔发生了 反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象是 ,乙炔发生了 反应。
(4)为了安全,点燃乙炔前应 ,乙炔燃烧时的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相同,Y和Z相邻,Z原子的最外层电子数是次外层电子数的三倍,则
(1)写出下列元素名称:X是_____,Z是_____.Y在周期表中第____周期,第_____族。
(2)由Y和Z组成,且Y和Z的质量比为7:20的化合物的分子式是______.
(3)写出由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子数的两种阴、阳离子______和______。
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子个数比为4:2:3,该盐的化学式是______;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com