
【题目】理论上不能设计为原电池的化学反应是
A. CH4(g)+2O2(g)==CO2(g)+2H2O(l)
B. HNO3(aq)+NaOH(aq)==NaNO3(aq)+H2O(l)
C. 2H2(g)+O2(g)==2H2O(l)
D. 2FeCl3(aq)+Fe(s)==3FeCl3(aq)
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】合成高分子化合物提高了人类的生活质量。下列说法正确的是
A. 涤纶、锦纶、蚕丝都属于合成纤维
B. 塑料、液晶高分子和合成橡胶被称为三大合成材料
C. 用于生产“尿不湿”的高吸水性树脂属于功能高分子材料
D. 酚醛树脂是酚类物质和醛类物质加聚而成的高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18克/厘米3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用下图所示装置制备1,2二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴(表面覆盖少量水)。请填写下列空白:
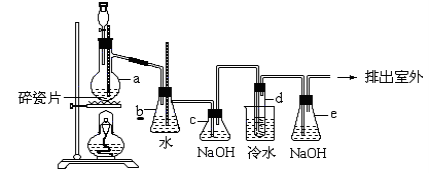
(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速高到170℃,否则容易产生副反应。请你写出乙醇的这个消去反应方程式:____________。
(2)写出制备1,2二溴乙烷的化学方程式: 。
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象: 。
(4)容器c中NaOH溶液的作用是: 。
(5)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因:___________。
(6)e装置内NaOH溶液的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电解质溶液的有关叙述正确的是( )
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)= c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)= c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B. 用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度
C. 用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率
D. 金属发生吸氧腐蚀时,被腐蚀的速率与氧气浓度无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机化合物相关的说法正确的是
A. 淀粉、油脂、蛋白质都能水解,但水解产物不同
B. 甲烷和Cl2、乙烯和Br2的反应类型相同
C. 1mol ![]() 与足量Na反应生成2molH2
与足量Na反应生成2molH2
D. 分子式为C4H10O,含有“-CH2OH”的有机物的同分异构体有3种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的某有机物和足量钠反应,可得Va L气体,等质量的该有机物如果与足量NaHCO3反应,同温同压得到Vb L气体,若Va=Vb,则该有机物可能是( )
A.HOCH2COOH B.HO—CH2CH2—CHO C.HOOC—COOH D.CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)被联合国世界卫生组织(WHO)列为AⅠ级高效安全灭菌消毒剂。常温下二氧化氯为黄绿色气体,其熔点为-59.5℃,沸点为11.0℃,能溶于水,不与水反应。温度过高,二氧化氯的水溶液可能爆炸。某研究性学习小组拟用下图所示装置制取并收集ClO2。(加热和夹持装置均省略)
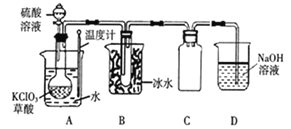
(1)在圆底烧瓶中先放入一定量的KClO3和草酸(H2C2O4),然后再加入足量的稀硫酸,在60℃~80℃之间生成C1O2、CO2和一种硫酸盐,该反应的化学方程式为____________________。
(2)A装置中使用温度计的目的________________。反应开始后,可以观察到圆底烧瓶内的现象是________。
(3)B装置的作用是______________。
(4)D装置中的NaOH溶液吸收尾气中的ClO2,生成物质的量之比为的1:1的两种盐,一种为NaClO2,另一种为________。
(5)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:量取ClO2溶液10.0mL,稀释成100.,0mL试样;量取V1mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,振荡后,静置片刻;
步骤3:加入指示剂X,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。
(已知:2ClO2+8H++10I-=5I2+2Cl-+4H2O;2Na2S2O3+I2=Na2S4O6+2NaI)
指示剂X为________。原ClO2溶液的浓度为_________g·L-1(用含字母的代数式表示)。
(6)有同学认为KC1O3在酸性条件下与草酸反应会生成KCl。请设计实验证明A装置反应后的溶液中是否存在C1-,简要写出所需试剂、实验操作、现象和结论。(已知:AgClO3可溶于水)
_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,有关下列溶液的说法不正确的是
A. 20mL0.1mol/LCH3COONa溶液与 10mL0.1mol/LHCl溶液混合后呈酸性,所得溶液中:
c(CH3COO-)c(Cl-)c(CH3COOH)c(H+)
B. 0.1mol/L Na2C2O4溶液与 0.1mol/L HCl 溶液等体积混合,所得溶液中:
2c(C2O42-)+c(HC2O4-)+ c(OH-)= c(Na+)+ c(H+)
C. 含等物质的量的NaHC2O4和Na2C2O4的溶液中:2 c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)]
D. 将amol/L氨水与0.01mol/L 盐酸等体积混合,若反应完全时溶液中 c(NH4+)=c(Cl-),则NH3·H2O的电离常数![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com