


分析 (1)Fe与溴反应生成溴化铁,苯和液溴在溴化铁作催化剂条件下能发生取代反应生成溴苯与HBr;
(2)溴苯中的溴易挥发,非极性分子的溶质易溶于非极性分子的溶剂,据此分析苯的作用;该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸能使石蕊试液变红色;氢溴酸能和硝酸银反应生成淡黄色沉淀溴化银;
(3)溴化铁与氢氧化钠反应生成氢氧化铁沉淀,氢氧化钠除去为反应的溴,溴苯与氢氧化钠溶液不互溶;
(4)HBr易溶于水,直接将导管伸入水溶液液面以下,会发生倒吸;
(5)本实验中进行尾气处理,防止污染空气;
(6)本实验中涉及的有机物主要是苯和溴苯,将B中的产物进行过滤,将滤液转移到分液漏斗中分液,将下层液体再次水洗分液而后进行干燥,最后得到的液体中主要含有的有机物就是苯和溴苯;
解答 解:(1)Fe与溴反应生成溴化铁,苯和液溴在溴化铁作催化剂条件下能发生取代反应生成溴苯与HBr,反应方程式为:2Fe+3Br2=2FeBr3, ,
,
故答案为:2Fe+3Br2=2FeBr3; ;
;
(2)溴苯中的溴易挥发,溴和四氯化碳都是非极性分子,根据相似相溶原理知,溴易溶于四氯化碳,所以四氯化碳的作用是吸收溴蒸汽;该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸是酸性物质,能使石蕊试液变红色;氢溴酸能和硝酸银反应生成淡黄色沉淀溴化银,所以观察D和E两试管,看到的现象是D管中变红,E管中出现浅黄色沉淀,
故答案为:除去HBr气体中混有的溴蒸气;D管中石蕊试液慢慢变红,并在导管口有白雾产生,而后E管中出现浅黄色沉淀;
(3)苯与液溴发生取代反应生成溴苯和溴化氢,溴苯是密度大于水,无色的油状液体,溴化氢易挥发,能与水蒸气结合成氢溴酸液滴,溴化铁与氢氧化钠反应生成红褐色的氢氧化铁沉淀,
故答案为:溶液中有红褐色的絮状物生成,底部有无色油状物质生成,液面上有白雾;
(4)HBr易溶于水,直接将导管伸入水溶液液面以下,会发生倒吸,装置D、E中导管口在液面上方,能防止倒吸,F中倒置漏斗增大了气体与氢氧化钠溶液的接触面积,有缓冲作用,能够防止倒吸,
故答案为:DEF;
(5)本实验中进行尾气处理,充分吸收有毒气体,防止大气污染,
故答案为:充分吸收有毒气体,防止大气污染;
(6)本实验中涉及的有机物主要是苯和溴苯,将B中的产物进行过滤,将滤液转移到分液漏斗中分液,将下层液体再次水洗分液而后进行干燥,最后得到的液体中主要含有的有机物就是苯和溴苯,
故答案为:苯和溴苯.
点评 本题考查了苯的取代反应实验,考查的知识点有反应方程式的书写、产物的判断、蒸汽的成分及性质,有一定的综合性,难度中等,注意苯能和液溴发生取代反应,和溴水不反应.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 2.4g金属镁所含电子数目为1.2NA | B. | 16g CH4所含原子数目为NA | ||
| C. | 17gNH3所含中子数目为10 NA | D. | 18g水所含分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ.在某温度时按n(N2):n(H2)=1:3的比例将混合气体投入密闭容器中反应:N2(g)+3H2(g)═2NH3(g)△H<0;
Ⅰ.在某温度时按n(N2):n(H2)=1:3的比例将混合气体投入密闭容器中反应:N2(g)+3H2(g)═2NH3(g)△H<0;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯甲酸是一种重要的化工产品,某学习小组设计方案制备苯甲酸.反应原理如下:
苯甲酸是一种重要的化工产品,某学习小组设计方案制备苯甲酸.反应原理如下: +2KMnO4$\stackrel{△}{→}$
+2KMnO4$\stackrel{△}{→}$ +KOH+2MnO2+H2O
+KOH+2MnO2+H2O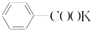 +HCl→
+HCl→ +KCl
+KCl
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱电解质的电离是一个吸热过程,升温其电离度增大 | |
| B. | 某些盐类的水解是一个吸热过程,升温水解程度增大 | |
| C. | 溶液的酸碱性取决于溶液中氢离子浓度的大小 | |
| D. | 酸性溶液不一定是酸溶液,碱性溶液不一定是碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


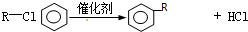
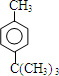 ;E
;E .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+有氧化性,实验室常用KSCN溶液检验Fe3+ | |
| B. | SO2有较强的还原性,SO2可使酸性KMnO4溶液褪色 | |
| C. | Mg有还原性,电解MgCl2饱和溶液可制备Mg | |
| D. | 浓H2SO4有吸水性,浓H2SO4可使蔗糖炭化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com