

 2S(s) + 2H2O(g) ¦¤H= £442.38 kJ/mol ¢Ł
2S(s) + 2H2O(g) ¦¤H= £442.38 kJ/mol ¢Ł SO2(g) ¦¤H=£297.04 kJ/mol ¢Ś
SO2(g) ¦¤H=£297.04 kJ/mol ¢Ś 2SO2(g)+2H2O(g) ¦¤H= £1036.46 kJ/mol £Ø·½³ĢŹ½ŗĶ¼ĘĖćø÷1·Ö£©
2SO2(g)+2H2O(g) ¦¤H= £1036.46 kJ/mol £Ø·½³ĢŹ½ŗĶ¼ĘĖćø÷1·Ö£© HSO3”Ŗ+ H+ HSO3”Ŗ
HSO3”Ŗ+ H+ HSO3”Ŗ SO3 2”Ŗ+ H+ £ØĆæøö1·Ö£©
SO3 2”Ŗ+ H+ £ØĆæøö1·Ö£© CO2 ”ü+ H2O£ØĪļÖŹ1·Ö£¬ÅäĘ½1·Ö£©
CO2 ”ü+ H2O£ØĪļÖŹ1·Ö£¬ÅäĘ½1·Ö£© HSO3”Ŗ+ H+ HSO3”Ŗ
HSO3”Ŗ+ H+ HSO3”Ŗ SO3 2”Ŗ+ H+ ÕżĻņŅĘ¶Æ£Ø1·Ö£©£¬Ģįø߶žŃõ»ÆĮņµÄ×Ŗ»ÆĀŹ£¬Ķ¬Ź±Ęšµ½¼Óæģ·“Ó¦ĖŁĀŹµÄ×÷ÓĆ£Ø1·Ö£©”£
SO3 2”Ŗ+ H+ ÕżĻņŅĘ¶Æ£Ø1·Ö£©£¬Ģįø߶žŃõ»ÆĮņµÄ×Ŗ»ÆĀŹ£¬Ķ¬Ź±Ęšµ½¼Óæģ·“Ó¦ĖŁĀŹµÄ×÷ÓĆ£Ø1·Ö£©”£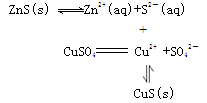
 SO4 2”Ŗ+ 4H+£ØĪļÖŹ1·Ö£¬ÅäĘ½1·Ö£©
SO4 2”Ŗ+ 4H+£ØĪļÖŹ1·Ö£¬ÅäĘ½1·Ö£© 2SO2(g)+2H2O(g) ¦¤H= £1036.46 kJ/mol
2SO2(g)+2H2O(g) ¦¤H= £1036.46 kJ/mol  HSO3”Ŗ+ H+ HSO3”Ŗ
HSO3”Ŗ+ H+ HSO3”Ŗ SO3 2”Ŗ+ H+
SO3 2”Ŗ+ H+  CO2 ”ü+ H2O
CO2 ”ü+ H2O HSO3”Ŗ+ H+ HSO3”Ŗ
HSO3”Ŗ+ H+ HSO3”Ŗ SO3 2”Ŗ+ H+ ÕżĻņŅĘ¶Æ£¬Ģįø߶žŃõ»ÆĮņµÄ×Ŗ»ÆĀŹ£¬Ķ¬Ź±Ęšµ½¼Óæģ·“Ó¦ĖŁĀŹµÄ×÷ÓĆ£»
SO3 2”Ŗ+ H+ ÕżĻņŅĘ¶Æ£¬Ģįø߶žŃõ»ÆĮņµÄ×Ŗ»ÆĀŹ£¬Ķ¬Ź±Ęšµ½¼Óæģ·“Ó¦ĖŁĀŹµÄ×÷ÓĆ£» Zn2+(aq)+S2£(aq)Ę½ŗā£¬µ±Óöµ½ĮņĖįĶČÜŅŗŹ±£¬S2£ÓėCu2+½įŗĻÉś³ÉCuS³Įµķ£¬Ź¹ČܽāĘ½ŗāÕżĻņŅĘ¶Æ£¬×īÖÕZnSČ«²æ×Ŗ»ÆĪŖCuS£¬ÓĆ»ÆѧÓĆÓļ±ķŹ¾ĪŖ
Zn2+(aq)+S2£(aq)Ę½ŗā£¬µ±Óöµ½ĮņĖįĶČÜŅŗŹ±£¬S2£ÓėCu2+½įŗĻÉś³ÉCuS³Įµķ£¬Ź¹ČܽāĘ½ŗāÕżĻņŅĘ¶Æ£¬×īÖÕZnSČ«²æ×Ŗ»ÆĪŖCuS£¬ÓĆ»ÆѧÓĆÓļ±ķŹ¾ĪŖ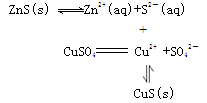
 SO4 2”Ŗ+ 4H+
SO4 2”Ŗ+ 4H+


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÓÉ°×Į×±äŗģĮ׏ĒĪüČČ·“Ó¦ |
| B£®°×Į×”¢ŗģĮ׶¼ŹĒĮ׵ĵ„ÖŹ£¬Ļą»„æÉŅŌ×ŌÓÉ×Ŗ»Æ£¬²»ĪüČČ£¬Ņ²²»·ÅČČ |
| C£®µČÖŹĮæŹ±£¬°×Į×±ČŗģĮ×¾ßÓŠµÄÄÜĮæøß |
| D£®µČĪļÖŹµÄĮæŹ±£¬¶Ļ°×Į×·Ö×ÓÖŠµÄ¼ü±Č¶ĻŗģĮ×·Ö×ÓÖŠµÄ¼üĻūŗĵÄÄÜĮæ¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĀČ»ÆÄĘ | B£®¹ĢĢåĻõĖįļ§ | C£®¹ĢĢåĒāŃõ»ÆÄĘ | D£®ÉśŹÆ»Ņ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ćŗ”¢ŹÆÓĶŗĶĢģČ»Ęų¶¼ŹōÓŚĢ¼ĖŲČ¼ĮĻ |
| B£®·¢Õ¹Ģ«ŃōÄܾ¼ĆÓŠÖśÓŚ¼õ»ŗĪĀŹŅŠ§Ó¦ |
| C£®Ģ«ŃōÄܵē³Ųæɽ«Ģ«ŃōÄÜÖ±½Ó×Ŗ»ÆĪŖµēÄÜ |
| D£®ÄæĒ°ŃŠ¾æ²¤²Ėµ°°×ÖŹ”°·¢µē”±²»ŹōÓŚ”°Ģ«ŃōÄÜĪÄĆ÷”± |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Éś³ÉĪļ×ÜÄÜĮæŅ»¶ØµĶÓŚ·“Ó¦Īļ×ÜÄÜĮæ |
B£®Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬H2(g)£«Cl2(g)£½2HCl(g) ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀµÄ H²»Ķ¬ H²»Ķ¬ |
C£®Ņ»¶ØĢõ¼žĻĀ£¬0.5 mol N2ŗĶ1.5 mol H2ÖĆÓŚÄ³ĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3Ęų£¬·ÅČČ19.3 kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖN2(g)£«3H2(g) 2NH3(g) 2NH3(g)  H =£38.6 kJ/mol H =£38.6 kJ/mol |
| D£®Ņ»¶ØĢõ¼žĻĀ4 HCl(g)£«O2(g)£½2Cl2(g)£«2H2O(g) £¬µ±1 mol |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®·“Ó¦Īļ±ČÉś³ÉĪļĪČ¶Ø | B£®øĆĶ¼æÉŅŌ±ķŹ¾ŹÆ»ŅŹÆøßĪĀ·Ö½ā |
| C£®øĆ·“Ó¦µÄ”÷H>0 | D£®ŅņĪŖÉś³ÉĪļµÄ×ÜÄÜĮæøßÓŚ·“Ó¦ĪļµÄ×ÜÄÜĮæøĆ·“Ó¦Ņ»¶ØŠčŅŖ¼ÓČČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®2N2H4(g)£«2NO2(g)£½3N2(g)£«4H2O(l)£»”÷H£½£1135.7 kJ/mol |
| B£®2N2H4(g)£«2NO2(g)£½3N2(g)£«4H2O(g)£»”÷H£½£1000.3 kJ/mol |
| C£®N2H4(g)£«NO2(g)£½3/2N2(g)£«2H2O(l)£»”÷H£½£1135.7 kJ/mol |
| D£®2N2H4(g)£«2NO2(g)£½3N2(g)£«4H2O(g)£»”÷H£½£1135.7 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®S(s£¬µ„Š±)=S(s£¬Õż½») ¦¤H£½£«0.33 kJ”¤mol£1 |
| B£®Õż½»Įņ±Čµ„Š±ĮņĪČ¶Ø |
| C£®ĻąĶ¬ĪļÖŹµÄĮæµÄÕż½»Įņ±Čµ„Š±ĮņĖłŗ¬ÓŠµÄÄÜĮæøß |
| D£®¢ŁŹ½±ķŹ¾¶ĻĮŃ1 mol O2ÖŠµÄ¹²¼Ū¼üĖłĪüŹÕµÄÄÜĮæ±ČŠĪ³É1 mol SO2ÖŠµÄ¹²¼Ū¼üĖł·Å³öµÄÄÜĮæÉŁ297.16 kJ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com