
 (Ⅰ)磷是生物体中不可缺少的元素之一,在自然界中磷总是以磷酸盐的形式出现的,例如磷酸钙矿Ca3(PO4)2、磷灰石Ca5F(PO4)3等.
(Ⅰ)磷是生物体中不可缺少的元素之一,在自然界中磷总是以磷酸盐的形式出现的,例如磷酸钙矿Ca3(PO4)2、磷灰石Ca5F(PO4)3等.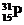 .
.分析 (Ⅰ)(1)P元素的原子序数是15,中子数比质子数多1,中子数为16,根据核素的表示方法来书写;
(2)酸性氧化物是能和碱反应生成盐和水的化合物;
(3)化合价降低元素所在的反应物是氧化剂,根据电子守恒来计算消耗的CuSO4的物质的量之比;
(Ⅱ)亚铁离子通过阳离子交换膜进入左边被盐酸酸化的H2O2氧化,铁离子通过阳离子交换膜进入右边与KSCN溶液接触,溶液变成血红色,当有2mol SO42-通过交换膜时,根据电荷守恒则有4molOH-进入左室,左室生成氢氧化铝$\frac{4}{3}$mol,右室生成2mol硫酸钡,则左右两室沉淀的物质的量之比为2:3;
(Ⅲ)根据题意,石墨中氧化物杂质均转变为相应的氯化物,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃;
(1)a应该是SiCl4,结合a与过量的NaOH溶液反应,可得两种盐,其中一种盐的水溶液具有粘合性(Na2SiO3);
(2)b是AlCl3、FeCl3、MgCl2的混合物,与过量的NaOH溶液充分反应后,过滤,所得滤液中阴离子有Cl-、OH-、AlO2-;
解答 解:(Ⅰ)(1)在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数,因为质子数和中子数之和是质量数,P元素的原子序数是15,中子数比质子数多1,所以质量数为15+15+1=31,所以表示该核素的原子符号为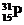
故答案为: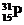
(2)能和碱反应生成盐和水的氧化物是酸性氧化物,所以属于酸性氧化物的是SiO2、P4O10,
故答案为:SiO2、P4O10;
(3)反应①中,硫酸铜中铜的化合价从+2价降低到+1价,得到电子,被还原,发生还原反应,因此硫酸铜是氧化剂,另外P元素的化合价从0价部分降低到-3价,得到电子,白磷也是氧化剂,如果被氧化的白磷都是1mol,则反应中转移电子是20mol,所以根据电子的得失守恒可知,反应①中需要硫酸铜是20/6×3=10mol.而在反应②需要硫酸铜是20×$\frac{1}{2}$=10mol,所以消耗的CuSO4的物质的量之比为1:1,
故答案为:CuSO4 和P4;1:1;
(Ⅱ)离子交换膜是一类具有离子交换功能的高分子材料.一容器被离子交换膜分成左右两部分,如图所示.若该交换膜为阳离子交换膜(只允许阳离子自由通过),左边充满盐酸酸化的H2O2溶液,右边充满滴有KSCN溶液的FeCl2溶液(足量),亚铁离子通过阳离子交换膜进入左边被盐酸酸化的H2O2氧化,铁离子通过阳离子交换膜进入右边与KSCN溶液接触,溶液变成血红色,离子方程式为:2H++2Fe2++H2O2=2H2O+2Fe3+,若该交换膜为阴离子交换膜(只允许阴离子自由通过),左边充满含2mol NH4Al(SO4)2的溶液,右边充满含3mol Ba(OH)2的溶液,当有2mol SO42-通过交换膜时(若反应迅速完全),当有2mol SO42-通过交换膜时,根据电荷守恒则有4molOH-进入左室,左室生成氢氧化铝$\frac{4}{3}$mol,右室生成2mol硫酸钡,则左右两室沉淀的物质的量之比为2:3;
故答案为:溶液由浅绿色变红色;2:3;
(Ⅲ)根据题意,石墨中氧化物杂质均转变为相应的氯化物,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃;
(1)a应该是SiCl4,结合a与过量的NaOH溶液反应,可得两种盐,其中一种盐的水溶液具有粘合性(Na2SiO3)得:SiCl4+6NaOH=Na2SiO3+4NaCl+3H2O;
故答案为:SiCl4+6NaOH=Na2SiO3+4NaCl+3H2O;
(2)b是AlCl3、FeCl3、MgCl2的混合物,与过量的NaOH溶液充分反应后,过滤,所得滤液中阴离子有Cl-、OH-、AlO2-;
故答案为:Cl-、OH-、AlO2-.
点评 本题考查学生核素和氧化还原反应中的基本概念知识、铝、铁、镁及化合物的性质,掌握题干信息和物质性质、注意电子守恒在氧化还原反应中的应用以及理解离子交换膜的作用是关键,题目难度中等.


 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:解答题
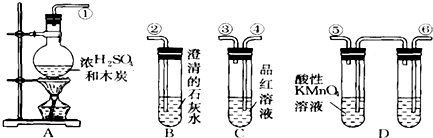
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所用氢氧化钠已经潮解 | |
| B. | 向容量瓶中加水未到刻度线 | |
| C. | 有少量氢氧化钠溶液残留在烧杯里 | |
| D. | 用带游码的托盘天平称2.4 gNaOH时误用了“左码右物”方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
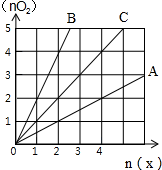
| A. | 2:1 | B. | 1:2 | C. | 1:1 | D. | 任意 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | M | N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
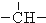 、
、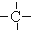 .如某烷烃分子中同时存在这四种基团,-CH2-、
.如某烷烃分子中同时存在这四种基团,-CH2-、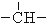 、
、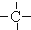 分别为m、n、a个,则该烷烃中-CH3的数目应是( )
分别为m、n、a个,则该烷烃中-CH3的数目应是( )| A. | 2m+3n+4a | B. | m+2n+2a | C. | n+2a+2 | D. | m+n+2a |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向无水乙醇中加入浓H2SO4,加热至170°C产生的气体通入酸性KMnO4溶液,红色褪去,证明生成的气体全部是乙烯 | |
| B. | 润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 | |
| C. | 某些强氧化剂如氯酸钾、硝酸钾等或其混合物不能研磨,否则可能引起爆炸 | |
| D. | 取5mL0.1mol•L-1KI溶液,滴加0.1mol•L-1FeCl3溶液5~6滴,继续加入2mLCCl4,充分振荡后静置,取上层溶液加KSCN溶液,无明显现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com