
【题目】甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是

A.丙与庚的原子序数相差3
B.气态氢化物的热稳定性:戊>己>庚
C.乙所在周期元素中,其简单离子的半径最大
D.乙的单质在空气中燃烧生成的化合物只含离子键
【答案】B
【解析】
戊的一种单质(金刚石)是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲的原子序数为6-3=3,即甲为Li,由元素在周期表中的相对位置图可知,乙为Na,丙为K,丁为Ca;丁与辛属同周期元素,由第ⅣA族元素可知,己为Si,庚为Ge,辛为Ga;
A.丙为K,K的原子序数为19,庚为Ge,Ge的原子序数为32,原子序数相差13,A项错误;
B.元素的非金属性越强,气态氢化物越稳定,同主族元素从上到下元素的非金属性逐渐减弱,则气态氢化物的热稳定性:戊>己>庚,B项正确;
C.根据上述分析,乙为Na,Na+有2个电子层,而同周期的S2-、Cl-有3个电子层,半径都比Na+大,所以Na+的半径不是最大,C项错误;
D.乙为Na,Na在空气中燃烧生成Na2O2,Na2O2中既有离子键、又有共价键,D项错误;
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某研究小组用如图所示装置模拟工业上生产无水FeCl2的过程。下列说法中正确的是( )

A.先点燃C处酒精灯,再打开分液漏斗的活塞
B.本实验中浓![]() 体现出吸水性和强氧化性
体现出吸水性和强氧化性
C.用D装置适合对该模拟实验进行尾气处理
D.C装置中的反应为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述不正确的是
A.淀粉![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B.纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C.油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D.蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“嫦娥飞天,玉兔登月”实现了中华民族“九天揽月” 的伟大梦想,“玉兔”号月球车上太阳能电池板使用的半导体材料是( )

A.硫B.硅C.镁D.铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林是常用的抗凝血药物。下面是利用 Michael 反应合成华法林的一种方法。
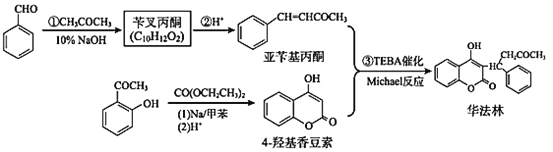
回答下列问题:
(1)![]() 的名称是_____。用银氨溶液检验其官能团的反应的化学方程式为________。
的名称是_____。用银氨溶液检验其官能团的反应的化学方程式为________。
(2)反应①~③中,属于加成反应的是_______(填序号)。
(3)苄叉丙酮的结构简式为 ______。
(4)![]() 中官能团的名称为_______、_______。
中官能团的名称为_______、_______。
(5)反应①除生成苄叉丙酮外,可能生成另一种化合物。该化合具有以下特征:
a.化学式为 C17H18O3;b.核磁共振氢谱有 6 组峰,且面积之比为 1:1:1:2:2:2;
则该化合物的结构简式为_________。
(6)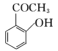 有多种同分异构体,属于芳香族化合物且为酯的同分异构体数目为 _______,其中不含“-CH3”的结构简式为 _______。
有多种同分异构体,属于芳香族化合物且为酯的同分异构体数目为 _______,其中不含“-CH3”的结构简式为 _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个1L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:

(1)从开始至2min,X的平均反应速率为__________;
(2)该反应的化学方程式为_______________________;
(3)1min时,正逆反应速率的大小关系为:v(正)_____v(逆),2min时,v(正)_____v(逆)。(填“>”或“<”或“=”)
(4)若X、Y、Z均为气体,在2min时,向容器中通入氩气,增大体系压强,X的化学反应速率将______,若加入适合的催化剂,Y的化学反应速率将______。(填“变大”或“不变”或“变小”)
(5)若X、Y、Z均为气体,下列能说明反应已达平衡的是_____________。
a.X、Y、Z三种气体的浓度相等
b.气体混合物物质的量不再改变
c.反应已经停止
d.反应速率v(X)︰v(Y)=2:1
e.(单位时间内消耗X的物质的量):(单位时间内消耗Z的物质的量)=3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中,用下图所示装置(尾气处理装置略去)进行下列实验,将①中液体逐滴滴入到②中。实验结果与预测的现象一致的是
选项 | ①中的物质 | ②中的物质 | 预测②中的现象 |
A. | 氢氧化钠 | 明矾溶液 | 开始时即产生白色沉淀 |
B. | 浓硫酸 | 铜片 | 产生无色气体,溶液变蓝 |
C. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
D. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 开始时无明显现象 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铵明矾(NH4Al(SO4)212H2O)是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备。用芒硝(Na2SO410H2O)制备纯碱和铵明矾的生产工艺流程图如图1:
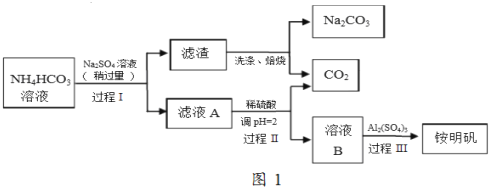
完成下列填空:
(1)铵明矾溶液呈_________性,它可用于净水,原因是_______________;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是__________________。
(2)写出过程Ⅰ的化学反应方程式_______________。
(3)若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是___________。
(4)已知铵明矾的溶解度随温度升高明显增大.加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、___________、过滤洗涤、干燥。
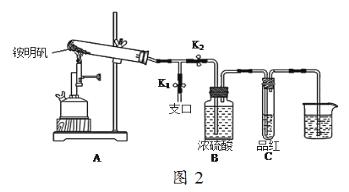
(5)某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份。
①夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是______________;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是___________(任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式_______________。
②该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为氢氧燃料电池的装置示意图,下列说法正确的是
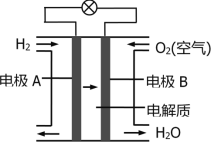
A. 该装置能将化学能转化为电能
B. 通入氧气的电极为负极
C. 电子由电极B经导线流向电极A
D. 正极反应式为:H2 – 2e- = 2H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com