
已知氟、氯、溴、碘、砹为同一主族元素,其中溴化砹(AtBr)可发生如下反应:
① 2AtBr + 2Mg = MgAt2 + MgBr2 ② AtBr + 2NH3 = NH4Br + AtNH2
对以上两个反应的有关说法中正确的是( )
A.这两个反应都是氧化还原反应
B.反应①中MgAt2既是氧化产物又是还原产物
C.反应②中AtBr既是氧化剂又是还原剂
D.MgAt2的还原性弱于MgBr2还原性
科目:高中化学 来源:2015届浙江省高三上学期第一次统练化学试卷(解析版) 题型:选择题
下列有关物质的性质与其应用不相对应的是
A.MgO、Al2O3的熔点很高,可制作耐高温材料
B.NaHCO3能与碱反应,食品工业上用作焙制糕点的膨松剂
C.Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
D.利用钠蒸气放电发光的性质制造的高压钠灯,可发出射程远、透雾能力强的黄光
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三10月月考化学试卷(解析版) 题型:选择题
下列离子或物质组能大量共存,且满足相应条件的是
选项 | 离子或物质 | 条件 |
A | Na+、K+、Cl-、SO42- | c(Na+)+c(K+)=c(SO42-)+ c(Cl-) |
B | Fe3+ 、SO32-、Cl- | 加入NaOH溶液,产生红褐色沉淀 |
C | Ba+ 、HCO3-、Cl-、H+ | 加入氨水产生沉淀 |
D | SO2、O2、NO2 | 通入足量NaOH溶液后,可能会没有任何气体剩余 |
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
取x g铜镁合金完全溶于浓硝酸中,若反应过程中HNO3被还原只生成NO、NO2,收集产生的气体,再通入0.56L氧气(标况),气体恰好可以被水吸收,在合金与HNO3反应后的溶液中加入足量的NaOH溶液可以生成3.9g沉淀,则x等于( )
A.1.2g B.2.2g C.3.2g D.无法计算
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
下列有关仪器的使用方法或实验操作正确的是( )
A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B.酸式滴定管装标准液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待测溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体。
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列判断正确的是( )
A.在18 g 18O2中含有NA个氧原子
B.标准状况下,22.4 L空气含有NA个单质分子
C.1 mol Cl2参加反应转移电子数一定为2 NA
D.含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol/L
查看答案和解析>>
科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:选择题
下列各组描述正确的是( )
A.化工生产要遵守三原则:充分利用原料、充分利用能量、保护环境。 ①燃烧时使用沸腾炉 ②制盐酸时将氯气在氢气中燃烧 ③制硫酸时使用热交换器 这3种化工生产分别符合以上某原则
B.①用燃烧的方法鉴别甲烷、乙烯和乙炔 ②用酒精萃取溴水中的溴 ③用水鉴别硝酸铵和氢氧化钠固体 ④用互滴法鉴别Na2CO3、盐酸、BaCl2、NaCl四种溶液 以上均能达到实验目的
C.①用硫粉覆盖地下撒有的汞 ②金属钠着火用泡沫灭火器或干粉灭火器扑灭 ③用热碱溶液洗去试管内壁的硫 ④用湿的红色石蕊试纸检验氨气是否集满 以上操作均合理
D.①过氧化氢:火箭燃料 ②碳酸氢钠: 食品发酵剂 ③钠:制氢氧化钠 ④硫酸:制蓄电池 以上物质的用途均合理
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:实验题
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
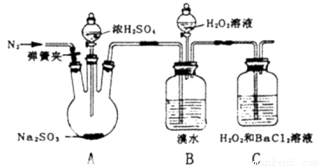
实验操作 | 实验现象 |
i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化,继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)A中发生反应的化学方程式是 .
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2.
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是 .
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是 .
③iii中滴入少量H2O2没有明显变化.提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是 .
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是 .
查看答案和解析>>
科目:高中化学 来源:2015届河南省高三9月第二次阶段考化学试卷(解析版) 题型:选择题
下列有关一定物质的量浓度的溶液配制的过程中,造成所得的溶液浓度偏大的是
A.要配制100 mL l mol/L NaOH溶液,需在白纸上称4 g NaOH固体,并且称量速度较慢
B.称量时托盘天平的砝码已被锈蚀
C.溶解或稀释溶质时烧杯尚未干燥
D.定容时盖上瓶盖,摇匀后发现液面低于刻度线,再继续滴加蒸馏水使液面重新达到刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com