
【题目】Ⅰ.回答下列问题:
(1)量子力学把电子在原子核外的一个空间运动状态称为一个________,还有一种状态叫做________。
(2)写出![]() 原子的外围电子排布式:______,其在周期表中的位置________,其在周期表中处于______区,与
原子的外围电子排布式:______,其在周期表中的位置________,其在周期表中处于______区,与![]() 同周期的所有副族元素的基态原子中,最外层电子数与
同周期的所有副族元素的基态原子中,最外层电子数与![]() 相同的元素有_________种。
相同的元素有_________种。
(3)下列![]() 原子电子排布图表示的状态中,能量最低和最高的分别为_______、_______(填标号)。
原子电子排布图表示的状态中,能量最低和最高的分别为_______、_______(填标号)。
A 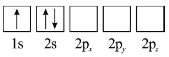 B
B 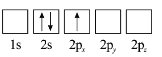
C 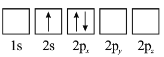 D
D 
Ⅱ.有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层![]() 能级的电子数等于次外层的电子总数, B元素可分别与A、C、D生成
能级的电子数等于次外层的电子总数, B元素可分别与A、C、D生成![]() 型化合物,并知在
型化合物,并知在![]() 中,
中,![]() 与
与![]() 的质量比为
的质量比为![]() 原子的价电子排布式为
原子的价电子排布式为![]() 。根据以上条件,回答下列问题:
。根据以上条件,回答下列问题:
(1)C的基态原子的电子占据最高能层的符号为_______,![]() 原子的价电子排布图________。
原子的价电子排布图________。
(2)A、B、C三种元素的第一电离能由大到小的顺序______(用元素符号表示)。
(3)元素B和D的电负性由大到小的顺序_________(用元素符号表示)。
(4)写出E的元素符号_________,要证明太阳光中含有E元素,可采用的方法是__________。
【答案】原子轨道 自旋 ![]() 第四周期第Ⅷ族
第四周期第Ⅷ族 ![]() 5 D C L
5 D C L ![]()
![]()
![]()
![]() 光谱分析
光谱分析
【解析】
Ⅰ.(1)量子力学把电子在原子核外的一个空间运动状态称为一个原子轨道,电子除空间运动状态外,还有一种运动状态叫做自旋;
(2)Fe为26号元素,Fe原子的电子排布式是1s22s22p63s23p63d64s2,据此分析解答;
(3)原子核外电子排布中,如果电子所占的轨道能级越高,该原子能量就越高;
Ⅱ.A原子最外层p能级的电子数等于次外层的电子数总数,p能级电子数不超过6,原子只能有2个电子层,则A的核外电子排布为1s22s22p2,故A为C元素;A、B、C属于同一周期,B元素可分别与A、C、D、E生成RB2型化合物,则B为O元素、C为N元素;在DB2中D与B的质量比为7∶8,则有Mr(D)∶2Mr(O)=7∶8,故Mr(D)=28,则D为Si元素;E原子的价电子排布式为3s23p6,则E为Ar,据此分析解答。
Ⅰ.(1)量子力学把电子在原子核外的一个空间运动状态称为一个原子轨道,电子除空间运动状态外,还有一种运动状态叫做自旋,故答案为:原子轨道;自旋;
(2)Fe为26号元素,原子的电子排布式是1s22s22p63s23p63d64s2,则其价电子排布式为:3d64s2,最高能级为4,价电子数为8,在周期表中位于第四周期第Ⅷ族;依据价电子排布可知处于d区;铁位于第四周期,最外层有2个电子,与铁同周期的所有副族元素的基态原子中,最外层电子数与铁相同的元素有Sc、Ti、V、Mn、Zn,共5种,故答案为:3d64s2;第四周期第Ⅷ族;d;5;
(3)原子核外电子排布中,如果电子所占的轨道能级越高,表明该原子能量越高,根据图知,电子排布能量最低的是1s、2s能级,能量最高的是2s、2p能级,故答案为:D;C;
Ⅱ. (1)C为N元素,其基态原子的电子占据最高能层的符号为L;B为O元素,其原子的价电子排布图为:![]() ,故答案为:L;
,故答案为:L;![]() ;
;
(2)同周期元素的第一电离能随着原子序数的增大而呈增大趋势,但N元素2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能大于同周期相邻元素,所以这三种元素的第一电离能从大到小顺序是:N>O>C,故答案为:N>O>C;
(3)同周期自左而右,主族元素的电负性增大,同主族自上而下,电负性呈减小趋势,故电负性:O>Si,故答案为:O>Si;
(4)E原子的价电子排布式为3s23p6,则E为Ar,要证明太阳光中含有E元素,可采用光谱分析,故答案为:Ar;光谱分析。


科目:高中化学 来源: 题型:
【题目】实验室石蜡催化裂化的装置如图所示,关于实验操作或叙述错误的是( )

A.试管Ⅰ连的玻璃导管加长是为使气态石蜡冷凝回流
B.装置Ⅱ中冷水的作用是冷凝收集裂化油
C.试管Ⅲ中溶液颜色变浅甚至褪色可说明有乙烯生成
D.酸性KMnO4溶液若倒吸可加快褪色速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离常数(25 ℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
①HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中阴离子结合质子能力最强的是__________。
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.H2SO4分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母) ___________。
③向NaCN溶液通入少量CO2反应的化学方程式是_____________________________。
(2)①一定浓度的NaCN溶液pH=9,用离子方程式表示呈碱性的原因是____________;此时c(HCN)/c(CN-)=____________。
②常温下,NaCN与过氧化氢溶液反应,生成NaHCO3和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。该反应的化学方程式是___________________________。
(3)已知CaCO3的Ksp=2.8×10-9,现将浓度为2×10-4 mol·L-1 Na2CO3溶液与CaCl2溶液等体积混合,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为_____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水四氯化锡常用作媒染剂和有机合成中的氯化催化剂。实验室可用熔融的锡(熔点 232 ℃)与 Cl2反应制备 SnCl4,装置如图。
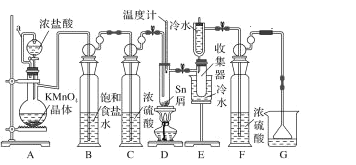
已知:①SnCl2、SnCl4 有关物理性质:
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
②SnCl4 极易水解生成 SnO2·xH2O。回答下列问题:
(1)导管 a 的作用是_____,装置 A 中发生反应的离子方程式为_____。
(2)当观察到装置 F 液面上方_____时才开始点燃 D 处的酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是①_________;②_____。
(3)若上述装置中缺少装置 C( 其它均相同) ,则D处具支试管中发生的主要副反应化学方程式为_____。
(4)Cl2和锡的反应产物有 SnCl4 和 SnCl2,为防止产品中带入过多的 SnCl2,可使用的温度范围是_____。
(5)滴定分析产品中 Sn(Ⅱ)的含量:用分析天平称取 5.000g 产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用 0.1000 mol·L-1 的碘标准溶液滴定至终点时消耗 20.00 mL,则产品中 Sn(Ⅱ)的含量为_____。(已知 Sn2++I2=2I-+Sn4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,混合溶液的
溶液,混合溶液的![]() 变化情况如图中所示曲线(体积变化忽略不计)。下列叙述正确的是( )
变化情况如图中所示曲线(体积变化忽略不计)。下列叙述正确的是( )
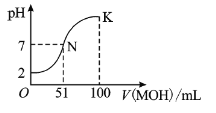
A.![]() 溶液的
溶液的![]() B.
B.![]() 点时加水稀释溶液,
点时加水稀释溶液,![]() 减小
减小
C.在![]() 点,
点,![]() D.在
D.在![]() 点,
点,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用“ Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,放电反应方程式为4Na+3CO2 =2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示,下列说法中错误的是( )
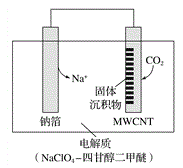
A. 电流流向为:MWCNT→导线→钠箔
B. 放电时,正极的电极反应式为 3CO2+4Na++4e-===2Na2CO3+C
C. 原两电极质量相等,若生成的Na2CO3和C全部沉积在电极表面,当转移0.2 mol e-时,两极的质量差为11.2g
D. 选用髙氯酸钠-四甘醇二甲醚做电解液的优点是导电性好,与金属钠不反应,难挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废气中的SO2经如图中的两个循环可分别得到S和H2SO4。下列说法正确的是
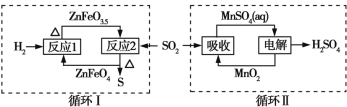
A. 循环Ⅰ中,反应1中的氧化产物为ZnFeO3.5
B. 循环Ⅰ中,反应2中的还原产物为ZnFeO4
C. Mn可作为循环Ⅱ中电解过程中的阳极材料
D. 循环Ⅰ和循环Ⅱ中消耗同质量的SO2,理论上得到S和H2SO4的质量之比为16∶49
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钠晶体 ![]() 俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿
俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿![]() 主要成份为
主要成份为![]() ,还含有
,还含有![]() 、MgO、
、MgO、![]() 等杂质
等杂质![]() 为主要原料进行生产,其主要工艺流程如下:
为主要原料进行生产,其主要工艺流程如下:
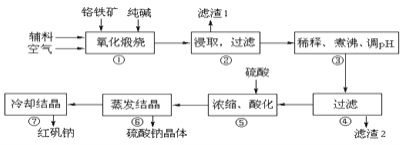
①中涉及的主要反应有:
主反应:![]()
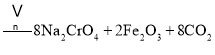
副反应: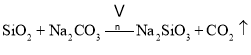 、
、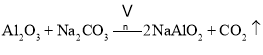
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
沉淀物 |
|
|
|
|
完全沉淀时溶液pH |
|
|
|
|
试回答下列问题:/span>
![]() “①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是 ______
“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是 ______
![]() “③”中调节pH至
“③”中调节pH至![]() ,目的是 ______ .
,目的是 ______ .
![]() “⑤”中加硫酸酸化的目的是使
“⑤”中加硫酸酸化的目的是使![]() 转化为
转化为![]() ,请写出该平衡转化的离子方程式: ______ .
,请写出该平衡转化的离子方程式: ______ .
![]() 称取重铬酸钠试样
称取重铬酸钠试样![]() 配成250mL溶液,取出
配成250mL溶液,取出![]() 于碘量瓶中,加入10mL
于碘量瓶中,加入10mL![]() 和足量碘化钠
和足量碘化钠![]() 铬的还原产物为
铬的还原产物为![]() ,放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用
,放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用![]() 标准溶液滴定
标准溶液滴定![]()
①判断达到滴定终点的依据是: ______ ;
②若实验中共用去![]() 标准溶液
标准溶液![]() ,所得产品的中重铬酸钠晶体的纯度
,所得产品的中重铬酸钠晶体的纯度![]() 设整个过程中其它杂质不参与反应
设整个过程中其它杂质不参与反应![]() ______ .
______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铬(Cr2O3)可用作有机合成的催化剂。某课题组以铬铁矿为主要原料制备Cr2O3。铬铁矿主要成分为Fe(CrO2)2,还含有Al2O3、SiO2等杂质,工艺流程如图所示。下列说法错误的是( )
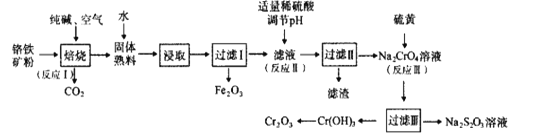
A.Fe(CrO2)2中Cr元素的化合价为+3
B.“焙烧”时,1molFe(CrO2)2参加反应转移4mole-
C.“滤渣”成份是Al(OH)3
D.“反应Ⅲ”的离子方程式为4CrO42-+6S+7H2O=4Cr(OH)3+3S2O32-+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com