
| A.Mg和O2 | B.NaOH和CO2 | C.Na2O2和CO2 | D.木炭(C)和O2 |
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源:不详 题型:计算题
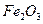 。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)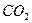 气体
气体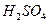 。溶液中,充分反应后,测得的实验数据如下表所示:
。溶液中,充分反应后,测得的实验数据如下表所示:| 实验序号 | I | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用稀盐酸洗去残留在试管壁上的铜 |
| B.用碱石灰吸收氨气中的水蒸气 |
| C.用稀盐酸清洗做焰色反应的铂丝 |
| D.用CCl4萃取碘水中的碘 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜在冷的浓硫酸中会钝化,所以把铜放入冷的浓硫酸中无明显现象 |
| B.NaOH溶液和AlCl3溶液相互滴加的现象不同 |
| C.金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
| D.Al.Fe.Cu三者对应的氧化物均为碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属镁着火,可用N2或CO2灭火 |
| B.MnO2、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸可以将它们区别开 |
| C.用洁净的玻璃棒蘸取某物质灼烧时,焰色反应为黄色,则该物质不一定只含钠元素 |
| D.用氯水、KSCN溶液可以检验硫酸亚铁溶液中亚铁离子的存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解质溶液中混入水,对电池反应无影响 |
| B.金属锂作电池的正极,石墨作电池的负极 |
| C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 |
| D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1 |
| A.工业上用铝单质与Fe2O3反应来大规模制备生铁 |
| B.可用焦碳与氧化铜高温反应制备铜 |
| C.古代“沙里淘金”是将金单质富积 |
| D.工业上由生铁炼钢以及由粗铜(含杂质较多的铜)制备纯铜都是进一步除去里面杂质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com