
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g)K=0.1。反应前CO的物质的量为10 mol,平衡后CO的物质的量为8 mol,下列说法正确的是( )
COS(g)+H2(g)K=0.1。反应前CO的物质的量为10 mol,平衡后CO的物质的量为8 mol,下列说法正确的是( )
A. 通入CO后,正反应速率逐渐增大
B. H2S的平衡转化率约为28.6%,CO的平衡转化率为80%
C. 平衡后H2S的质量为170 g
D. 升高温度,H2S浓度增加,表明该反应的逆反应是放热反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】H2S 和SO2 会对环境和人体健康带来极大的危害,工业上采取多种方法来减少这些有害气体的排放。
I.H2S 的除去
方法1: 生物脱H2S,反应的原理为H2S + Fe2(SO4)3==S↓+2FeSO4+H2SO4、4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3 +2H2O。
2Fe2(SO4)3 +2H2O。
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105 倍,该菌的作用是______。
(2)由图1和图2 判断,使用硫杆菌的最佳条件为_________。若反应温度过高,反应速率下降,其原因是______________。
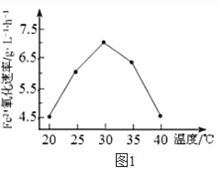
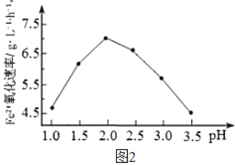
方法2: 在一定条件下,用H2O2 氧化H2S
(3)随着参加反应的n(H2O2)/n(H2S) 变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物 的分子式为________。
II.SO2 的除去
方法1( 双碱法): 用NaOH 吸收SO2 ,并用CaO 使NaOH 再生:NaOH 溶液![]() Na2SO3
Na2SO3
(4)写出过程①的离子方程式:_________________。
(5)CaO 在水中存在如下转化:CaO(s)+H2O(1)= Ca(OH)2(s)![]() Ca2+(aq) +2OH- (aq)。从平衡移动的角度,简述过程②NaOH再生的原理:_______________。
Ca2+(aq) +2OH- (aq)。从平衡移动的角度,简述过程②NaOH再生的原理:_______________。
方法2:用氨水除去SO2
(6)已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0mol/L,溶液中的c(OH-)=________。将SO2 通入该氨水中,当c(OH-)降至1.0×10-7mol/L时,溶液中的c (SO32-)/c(HSO3-) =_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到目的的是
选项 | 目 的 | 实 验 |
A | 加快稀溶液中草酸与KMnO4的反应 | 向溶液中加入少量MnSO4固体 |
B | 检验海带中的碘元素 | 向海带灰浸取液中滴加淀粉溶液 |
C | 除去食盐水中的少量BaCl2 | 向食盐水中通入过量的CO2 |
D | 制备少量氨气 | 将硝酸铵与氢氧化钙固体混合加热 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 淀粉、蛋白质和油脂都属于高分子化合物,一定条件下都能水解
B. 医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于水
C. 用过滤的方法从碘的四氯化碳溶液中获得碘
D. 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过硫酸氢钾复盐(化学式表示为K2SO4·KHSO4·2KHSO5),—般用作漂白剂及NOx、SO2等废气脱除剂。制备过硫酸氢钾复盐流程如图:
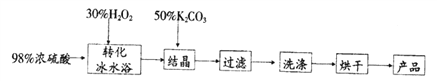
(1)在“转化”操作前,需先用冰水冷却双氧水,可能的原因是________________。“转化”过程中,浓硫酸与H2O2发生可逆反应生成过硫酸(H2SO5),写出该变化的化学反应方程式____________________。
(2)已知H2SO5为一元强酸。结晶操作中,加入K2CO3即可获得过硫酸氢钾复盐晶体,该过程的离子反应方程式为________________________;操作中,选用50%K2CO3溶液且需分批缓慢加入目的是____________。过硫酸氢钾复盐产率(以产品含氧量表示)随溶液pH和温度的变化关系如图所示。则该过程适宜的条件是________________。

(3)过滤后,用无水乙醇取代蒸馏水洗涤沉淀,目的是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新浪科技网最新报道:美科学家发现,普通盐水在无线电波的照射下可以燃烧,这很可能是人类最伟大的发现之一,有望解决未来人类的能源危机。无线电频率可以降低盐水中所含元素之间的结合力,释放出氢原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述“结合力”的实质是( )
A. 共价键 B. 离子键
C. 一种静电引力 D. 一种静电斥力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )
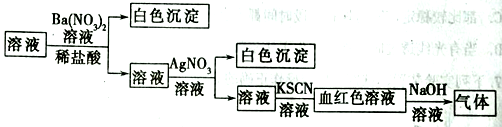
A.原溶液中一定含有SO42- B.原溶液中一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组探究氢气还原氧化铜的反应,部分实验装置如下:
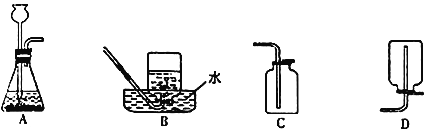
(1)上述A装置可用于实验室制取氢气、氧气、二氧化碳、二氧化硫等气体,请写出能用装置A制取氧气的化学方程式________________________________。上述可用于收集氧气装置是_______________(用装置字母序号填空)。
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ、氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);
Ⅱ、Cu和Cu2O均为不溶于水的红色固体;
Ⅲ、Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三:_______________________________________(请补充完成假设三)。
②实验探究:(将实验现象填写入表中空格)
实验操作 | 实验现象 | 实验结论 |
a、取少量红色固体加入到足量硫酸溶液中 | _________________________ | 假设一成立 |
b、取少量红色固体加入到足量硫酸溶液中 | __________________________ | 假设二或假设三成立 |
③若出现b中现象时因无法确定是假设二或是假设三成立,所以应进行进一步的数据处理:甲同学称取w g红色固体加入到足量硫酸溶液中使其充分反应后,__________(填操作名称)、洗涤、干燥,称量剩余红色固体质量为mg,通过计算:若m的取值范围为:w > m >______________,则假设三成立;
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属.三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出). 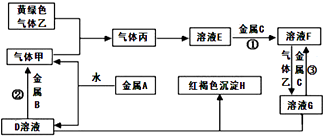
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙、H;
(2)写出反应②的离子方程式:;
(3)写出金属A与水反应的离子方程式;
(4)F与D溶液反应后的产物在空气中转化为H的化学方程式;现象为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com