
写出下列物质在水中电离的方程式:
NaOH H2SO4 .
考点:
电离方程式的书写.
专题:
电离平衡与溶液的pH专题.
分析:
强电解质在水溶液里完全电离生成阴阳离子,电离方程式写“=”,弱电解质在水溶液里部分电离,电离方程式写“⇌”,书写时要遵循原子守恒、电荷守恒,据此分析解答.
解答:
解:NaOH是强电解质,在水溶液里完全电离生成钠离子、氢氧根离子,电离方程式为:NaOH=Na++OH﹣,
H2SO4是强电解质,在水溶液里完全电离生成氢离子、硫酸根离子,电离方程式为:H2SO4=2H++SO42﹣,
故答案为:NaOH=Na++OH﹣;H2SO4=2H++SO42﹣.
点评:
本题考查了电离方程式的书写,明确电解质的强弱及电离方程式的书写规则是解本题关键,注意原子团不能拆开,题目难度不大.


科目:高中化学 来源: 题型:
NA为阿伏加德罗常数,下列叙述正确的是( )
|
| A. | 标准状况下,含NA个氩原子的氩气的体积约为11.2 L |
|
| B. | 31g白磷分子中,含有的共价单键数目是NA个 |
|
| C. | 6 g金刚石晶体中含有的碳碳键数目为2×6.02×1023 |
|
| D. | 4.5 g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的离子方程式或化学方程式
(1)Ba(OH)2与H2SO4反应:(离子方程式) ;
(2)Fe与HCl反应:(离子方程式) ;
(3)Al与HCl溶液反应:(化学方程式) .
查看答案和解析>>
科目:高中化学 来源: 题型:
在温度压强不变的情况下,已知N2O4⇌2NO2,2mol N2O4在密闭容器内分解成NO2,到达平衡时生成了0.6mol NO2,则平衡时气体的总物质的量是( )
|
| A. | 0.6mol | B. | 1.8mol | C. | 2.2mol | D. | 2.3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
100℃时,KW=1×10﹣12,对纯水的叙述正确的是( )
|
| A. | pH=6显弱酸性 | B. | C(H+)=10﹣6mol/L,溶液为中性 |
|
| C. | KW是常温时的10﹣2倍 | D. | 温度不变冲稀10倍pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
阅读下列实验内容,根据题目要求回答问题.
某学生为测定未知浓度的硫酸溶液,实验如下:以0.14mol•L﹣1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL.
(1)该学生用标准0.14mol•L﹣1NaOH溶液滴定硫酸的实验操作如下:
A、检查滴定管是否漏水
B、用蒸馏水洗干净滴定管
C、取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2﹣3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
D、用待测定的溶液润洗酸式滴定管
E、用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入指示剂.
F、把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G、另取锥形瓶,再重复操作一次
①该滴定操作中应选用的指示剂是 ;
②在F操作中如何确定终点? .
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入 (选填“甲”或“乙”)中.
(3)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”) .
(4)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值 (选填“偏大”“偏小”或“无影响”)

查看答案和解析>>
科目:高中化学 来源: 题型:
在不同条件下分别测得2SO2+O2⇌2SO3的化学反应速率,其中表示该反应进行最快的是( )
|
| A. | υ(SO2)=4 mol/(L•min) | B. | υ(O2)=0.1 mol/(L•s) |
|
| C. | υ(O2)=3mol/(L•min ) | D. | υ(SO2)=0.1 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
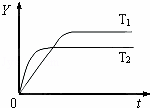
已知反应2SO2(g)+O2(g)⇌2SO3(g)△H<0,向某体积恒定的密闭容器中按体积比2:1充入SO2和O2,在一定条件下发生反应.下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )
|
| A. | SO2的转化率 | B. | 混合气体的密度 |
|
| C. | 密闭容器内的压强 | D. | O2的体积分数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com