
����Ŀ���⻯����ҽ�Ƽ�ʳƷ��������Ҫ�����á�ʵ������NaOH�����ʵ��ˮ����(N2H��H2O)Ϊԭ���Ʊ��⻯�ơ���֪��ˮ���¾��л�ԭ�ԡ��ش��������⣺
(1)ˮ���µ��Ʊ��йط�Ӧԭ��Ϊ��CO(NH2)2(����)+NaClO+2NaOH![]() N2H4��H2O+NaCl+Na2CO3
N2H4��H2O+NaCl+Na2CO3
����ȡ�������ƺ��������ƻ��Һ������˳��Ϊ__________(������������Сд��ĸ��ʾ)��
����ʵ���¶ȿ��Ʋ�������Ӧ��������ƿ��ClO-��ClO3-�����ʵ���֮��Ϊ5��1�����������������Ʒ�Ӧʱ������ԭ����Ԫ���뱻��������Ԫ�ص����ʵ���֮��Ϊ________��
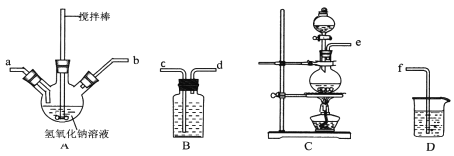
���Ʊ�ˮ����ʱ��Ӧ��___________�ε� __________ �У�����NaClO��Һ������������Һ�������ҵμ��ٶȲ��ܹ��졣
(2)�⻯�Ƶ��Ʊ�����ˮ���»�ԭ����ȡ�⻯�ƹ��壬���Ʊ�������ͼ��ʾ��
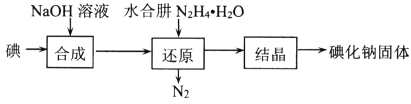
������ԭ�������У���Ҫ���ķ�Ӧ���������ɵĸ�����IO3-���ù��̵����ӷ���ʽΪ______________________________________����ҵ��Ҳ���������ƻ���м��ԭ�������Ʊ��⻯�ƣ���ˮ���»�ԭ���ƵõIJ�Ʒ���ȸ��ߣ���ԭ����_________________________________��
(3)�ⶨ��Ʒ��NaI������ʵ�鲽�����£�
a����ȡ10��00g��Ʒ���ܽ⣬��500mL����ƿ�ж��ݣ�
b����ȡ25��00mL����Һ����ƿ�У�Ȼ�����������FeCl3��Һ����ַ�Ӧ���ټ���M��Һ��ָʾ����
c����0��2100mol��L-1��Na2S2O3����Һ�ζ����յ�(��Ӧ����ʽΪ��2Na2S2O3+I2=Na2S4O6+2NaI)���ظ�ʵ���Σ�������ı���Һ�����Ϊ15��00mL��
��MΪ____________(д����)��
�ڸ���Ʒ��NaI����������Ϊ_______________��
���𰸡�ecdabf 5:3 NaClO��Һ ���� 2IO3-+3N2H4H2O=3N2��+2I-+9H2O N2H4H2O��������IJ���ΪN2��H2O������������ ���� 94.5%
��������
(1)�ٸ����Ʊ����������ӣ��Ʊ��������ƺ��������ƣ�����β������������ƿ��ClO-��ClO3-�����ʵ���֮��Ϊ5��1����ClO-��ClO3-�����ʵ����ֱ�Ϊ5mol��1mol�����ݵ�ʧ�����غ㣬����5molClO-�������Cl-5mol������1mol ClO3--�������Cl-5mol���ݴ˷����ɵã�
��NaClO����ˮ���£�
(2)���NaOH��Ӧ����NaI��NaIO��������IO3-������ˮ���»�ԭNaIO��������IO3-���õ������Ӻ͵������ᾧ�õ��⻯�ƣ�
(3)�ٵ�����Һ���ⵥ����Һ����ɫ��
�ڸ��ݵ�Ԫ���غ㣬2I-��I2��2Na2S2O3����n(NaI)=n(Na2S2O3)������Ʒ��NaI������Ϊ��0.2100mol��0.015L��![]() ��150g/mol=9.45g���ݴ˼��㡣
��150g/mol=9.45g���ݴ˼��㡣
(1)ˮ���µ��Ʊ��йط�Ӧԭ��Ϊ��CO(NH2)2(����)+NaClO+2NaOH![]() N2H4��H2O+NaCl+Na2CO3
N2H4��H2O+NaCl+Na2CO3
��װ��c�ɶ������Ǻ�Ũ�����Ʊ���������Bװ�õı���ʳ��ˮ��ȥHCl���壬Ϊ��֤���ӳ�֣������ܳ����̳���������NaOH��A�з�Ӧ�Ʊ���Ϊ��ַ�Ӧ����a��ȥ����Dװ������δ��Ӧ����������ֹ��Ⱦ�������ʵ���������˳��Ϊ��ecdabf������ƿ��ClO-��ClO3-�����ʵ���֮��Ϊ5��1����ClO-��ClO3-�����ʵ����ֱ�Ϊ5mol��1mol�����ݵ�ʧ�����غ㣬����5molClO-�������Cl-5mol������1mol ClO3-�������Cl-5mol����ԭ����Ԫ��Ϊ���ϼ۽��͵���Ԫ�أ���ΪCl-����5mol+5mol=10mol������������Ԫ��Ϊ���ϼ����ߵ���Ԫ�أ����ʵ���֮��ΪClO-��ClO3-��5mol+1mol=6mol���ʱ���ԭ����Ԫ���뱻��������Ԫ�ص����ʵ���֮��Ϊ10��6=5:3��
�ڽ����صε�NaClO��Һ�л����μӣ�����ʹ������NaClO��Һ����ˮ���£����Ͳ��ʣ���ʵ����ȡ����NaClO��Һ��μ��뵽������������Һ���Ʊ�ˮ���£��μ�˳���ܵߵ����ҵμ��ٶȲ��ܹ��죬��ֹˮ���±�������
(2)�������̿�֪��������IO3-��ˮ�������ɵ����Ӻ͵�������ӦΪ��2IO3-+3N2H4H2O=3N2��+2I-+9H2O��N2H4H2O��������IJ���ΪN2��H2O�����������ʣ�ˮ���»�ԭ���ƵõIJ�Ʒ���ȸ��ߣ�
(3)��ʵ���еζ��ⵥ�ʣ��õ�����ָʾ������MΪ���ۣ�
�ڸ��ݵ�Ԫ���غ㣬2I-��I2��2Na2S2O3����n(NaI)=n(Na2S2O3)������Ʒ��NaI������Ϊ��0.2100mol��0.015L��![]() ��150g/mol=9.45g��������������Ϊ
��150g/mol=9.45g��������������Ϊ![]() ��100%=94.5%��
��100%=94.5%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20 ��ʱ�������Ȼ�����Һ���ܶ�Ϊ1.174 g/mL�����ʵ���Ũ��Ϊ4.0 mol/L��������˵������ȷ����
A.25 ��ʱ�������Ȼ�����Һ��Ũ��С��4.0 mol/L
B.����Һ���Ȼ��ص���������Ϊ![]() ��100%
��100%
C.20 ��ʱ���ܶ�С��1.174 g/mL���Ȼ�����Һ�Dz�������Һ
D.������Һ��������ˮ���ٻָ���20 ��ʱ����Һ�ܶ�һ������1.174 g/mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ��X��Y��Z��W��ԭ�������������ӣ��Ҿ�������20��X�ĵ������ֻ������Ҫ�ĵ缫���ϣ������£�Y��������̬������֮��ɷ������淴Ӧ��X��Y��W����������֮����Z��������������ȣ�W���γɶ������������˵����ȷ����
A.�����£�Z�ĵ�����Y�ļ��⻯�����������ܲ�������
B.Z�ǽ�����ǿ��Y�����Ӧ����������ԣ�Z��Y
C.ԭ�Ӱ뾶��X��Y�������Ӱ뾶��Z<W
D.X��W�ĵ��ʾ�Ϊ���ý�����ͨ��������ú����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���¶�T1��T2ʱˮ�ĵ���ƽ��������ͼ��ʾ������˵���������(����)
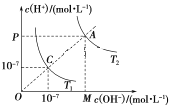
A.ˮ�����ӻ�������ϵΪ��C��A
B.�����¶ȿ�ʵ����C�㵽A��
C.T2ʱ��pH��4��������pH��10������������Һ�������ϣ�������Һ��pH��7
D.ͼ�о���OMAP�������ʾT2ʱˮ�����ӻ���ֵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Ԫ����B(OH)2(K1=5.9��10-2��K2=6.4��10-5)����10mLϡB(OH)2��Һ�еμӵ�Ũ��������Һ��B(OH)2��B(OH)+��B2+��Ũ�ȷ���������ҺPOH[POH=-lgc(OH)-]�仯�Ĺ�ϵ��ͼ������˵����ȷ����
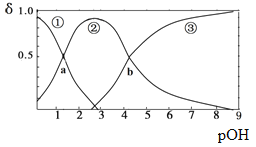
A. ����a����Ӧ�����������Һ�����Ϊ5mL
B. �������������Һ�����Ϊ10mLʱ����c(Cl-)>c(B(OH)+)>c(H+)>c(OH-)>c(B2+)
C. ����b��c(OH)=6.4��10-5
D. �������������Һ�����Ϊ15mLʱ���ڣ�c(Cl-)+c(OH-)= c(B2+)+c(B(OH)+)+ c(H+)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������̶������Ϊ1 L�ܱ��������Բ�ͬ����̼��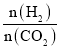 ����H2��CO2����һ�������·�����Ӧ��2CO2(g)+6H2(g)
����H2��CO2����һ�������·�����Ӧ��2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g)����H��CO2��ƽ��ת������(CO2)���¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ���� ( ��)
C2H4(g)+4H2O(g)����H��CO2��ƽ��ת������(CO2)���¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ���� ( ��)
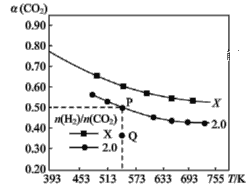
A.�÷�Ӧ�ڳ����²������Է�����
B.��̼�ȣ�X<2.0
C.����ʼʱCO2��H2Ũ�ȷֱ�Ϊ0.5 mol��L��1��1.0 mol��L��1����ɵ�P���Ӧ�¶ȵ�ƽ�ⳣ����ֵΪ512
D.��P��״̬�������У���2��4��1��4�ı����ٳ���CO2��H2��C2H4��H2O���ٴ�ƽ�����(CO2)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ��0.1 mol��L��1HA��Һ�� ��108��0.01 mol��L��1BOH��ҺpH��12����ش��������⣺
��108��0.01 mol��L��1BOH��ҺpH��12����ش��������⣺
��1��HA�ĵ��볣��KaΪ________��BOH��________(����ǿ��������������������)��
��2��pH��ȵ�BOH��Һ��BA��Һ���ֱ���ȵ���ͬ���¶Ⱥ�BOH��Һ��pH________(����������������������)BA��Һ��pH��
��3����֪̼���Ka1��4.3��10��7��Ka2��5.6��10��11�����Ũ�ȵ�Na2CO3��NaA����Һ�еμ�����ֱ������������H�����õ���������Ϊ___________________��
��4��25 ����������ĵ���ƽ�ⳣ�����±���
Ka1 | Ka2 | |
H2SO3 | 1.3��10��2 | 6.3��10��8 |
H2CO3 | 4.2��10��7 | 5.6��10��11 |
��HSO3-�ĵ���ƽ�ⳣ������ʽK��___________________��
��0.10 mol��L��1 NaHSO3��Һ������Ũ���ɴ�С��˳��Ϊ_____________________��
��H2SO3��Һ��NaHCO3��Һ��Ӧ����Ҫ���ӷ���ʽΪ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʯ�����Ҫ�ɷ�ΪFe3O4��Al2O3��MnCO3��MgO����MnO2�ȡ���ҵ�Ͻ�����ʯ����������������Ĥ��ⷨ���¼�����ȡ�����̲��Ƶ���ɫ��Ч��ˮ������(K2FeO4)����ҵ�������£�
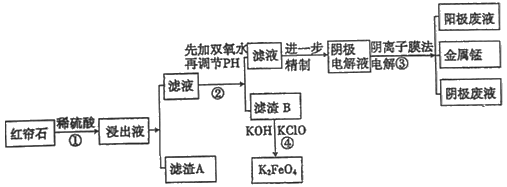
��1����ϡ�����ȡ��ʯ�Ĺ����У�MnO2�ɽ�Fe2+����ΪFe3+��д���÷�Ӧ�����ӷ���ʽ��___________________��
��2������Һ�е������ӳ�H+��Fe2+��Fe3+���_____________(�����ӷ���)��
��3����֪��ͬ����������������������������pH���±���
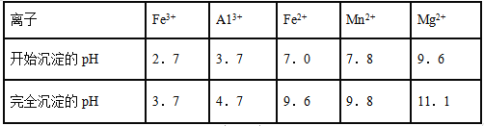
�������е�����Һ��pH����6������pH���Լ����ѡ�����������Լ�__________(��ѡ����ĸ����ͬ)����B�������ʺ�ɽ�һ����ȡK2FeO4����������B���������ѡ�����������Լ���________��
a. ϡ���� b. KOH c. ��ˮ d. MnCO3 e. CaCO3
��4������B����Ӧ�����ɸ�Чˮ�����������ӷ���ʽ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ԭ��ǿ����I����Fe2������100 mL�⻯������Һ�л���ͨ��3.36 L(��״��)��������Ӧ��ɺ���Һ����һ���Fe2+��������Fe3+����ԭ�⻯������Һ�����ʵ���Ũ��Ϊ
A. 1.2 mol��L��1 B. 1.5 mol��L��1 C. 1.0 mol��L��1 D. 1.1 mol��L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com