
【题目】可以将反应E+B2+=E2++B设计成原电池,下列4个电极反应: ①B﹣2e﹣=B2+
②E﹣2e﹣=E2+
③B2++2e﹣=B
④E2++2e﹣=E
其中表示负极反应和正极反应的分别是( )
A.②和③
B.②和①
C.③和①
D.④和①
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】[化学一物质结构与性质]
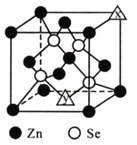
硒化锌是一种半导体材料,回答下列问题。
(1)锌在周期表中的位置_____________;Se基态原子价电子排布图为___________。元素锌、硫和硒第一电离能较大的是______________________(填元素符号)。
(2)Na2SeO3分子中Se原子的杂化类型为___________;H2SeO4的酸性比H2SeO3强,原因是_________________________________________________。
(3)气态SeO3分子的立体构型为__________;下列与SeO3互为等电子体的有____(填序号)。
A.CO32- B.NO3- C.NCl3 D.SO32-
(4)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为_____(填元素符号);该晶胞中硒原子所处空隙类型为______________(填“立方体”、“正四面体”或正八面体”),该种空隙的填充率为____________;若该晶胞密度为pg·cm-3,硒化锌的摩尔质量为Mg·mol-1。用NA代表阿伏加德罗常数的数值,则晶胞参数a为_____nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白头翁素衍生物H是一种具有抗菌作用的化合物,实验室由芳香化合物A制备H的一种合成路线如下:
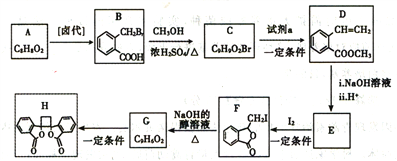
已知:i.RCH2Br![]() R-CH=CH-R
R-CH=CH-R
ii.2R-CH=CH-R'![]()
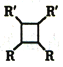 (以上R、R'代表氢或烃基等)
(以上R、R'代表氢或烃基等)
(1)A的化学名称是_____________。C中所含官能团的名称为_______________。
(2)试剂a是____________________,G生成H的反应类型是_____________________。
(3)由F生成G的化学方程式是_______________________________。
(4)D的同分异构体中,能同时满足下列条件的共有_______种(不含立体结构);
①苯环上只有两个取代基
②能使溴的四氯化碳溶液褪色
③既能发生银镜反应又能发生水解反应且水解产物之一能与氯化铁溶液发生显色反应,其中核磁共振氢谱为五组峰的有机物的结构简式为_________________________。
(5)以乙醇为起始原料,结合已知信息选用必要的无机试剂合成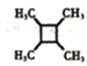 ,写出合成路线_________________(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线_________________(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1 mol氢气的化学键消耗的能量为Q1 kJ,破坏1 mol氯气的化学键消耗的能量为Q2kJ ,形成1 mol氯化氢的化学键释放的能量为Q3kJ,下列关系式正确的是
A. Q1 + Q2 > Q3 B. Q1 + Q2 < Q3 C. Q1 + Q2 > 2Q3 D. Q1 + Q2 < 2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝石墨双离子电池是一种全新低成本、高效电池。原理为:A1Li+Cx(PF6)![]() Al+xC+Li++PF6-。电池结构如图所示。下列说法正确的是
Al+xC+Li++PF6-。电池结构如图所示。下列说法正确的是

A. 放电时,外电路中电子向铝锂电极移动
B. 放电时,正极反应为Cx(PF6)+e-=xC+PF6-
C. 充电时,应将铝石墨电极与电源负极相连
D. 充电时,若电路中通过1 mol电子,阴极质量增加9 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家哈伯从1902 年开始研究由氮气和氢气直接合成氨,反应原理为:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJmol-1
2NH3(g) △H=-92.4kJmol-1
(1)在恒温恒容条件下,向反应平衡体系中充入氮气,达到新平衡时,c(H2)将_________(填“增大”、“减小”、“不变”或“无法判断”,下同),c(N2)·c3(H2)将___________。
(2)工业上可用CH4与水蒸气制氢气:CH4(g)+H2O(g)![]() CO(g)+3H2(g)。在200℃时2L的密闭容器中,将1molCH4和1mol H2O(g)混合,达平衡时CH4 的转化率为80%。则200℃时该反应的平衡常数K=______________(保留一位小数)。
CO(g)+3H2(g)。在200℃时2L的密闭容器中,将1molCH4和1mol H2O(g)混合,达平衡时CH4 的转化率为80%。则200℃时该反应的平衡常数K=______________(保留一位小数)。
(3)如图为合成氨反应在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积比为1:3 时,平衡混合物中氨的体积分数。若分别用vA(NH3)和vB(NH3)表示从反应开始至达平衡状态A、B 时的化学反应速率,则vA(NH3)____ ( 填“>”“<”或“=”)vB(NH3)。

(4)工业生产中逸出的氨可用稀硫酸吸收。若恰好生成NH4HSO4,该溶液中各离子的物质的量浓度由大到小的顺序是______________________。
(5)H2NCOONH4是工业合成尿素的中间产物,该反应的能量变化如图所示,用CO2和氨合成尿素的热化学方程式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮及其化合物与生活密切相关。请根据要求回答下列问题:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H=-l160kJ/mol
③H2O(g)= H2O(l) △H=-44kJ/mol
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O( 1) 的热化学方程式_________。
(2)已知: 反应I: 4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) △H < 0
4NO(g)+6H2O(g) △H < 0
反应II: 4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) △H < 0
2N2(g)+6H2O(g) △H < 0
①在恒温恒容装置中充入一定量的NH3 和O2,在催化剂的作用下进行反应I,则下列有关叙述中正确的是___(填字母序号)。
A.增大压强,Kp(用压强表示的化学平衡常数) 增大
B.若测得容器内3v正(NH3)=2v逆(H2O) 时,说明反应已达平衡
C.升高温度,NH3 的转化率增大
D.达到平衡时体系的压强不再变化
②氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1molNH3和2molO2,得有关物质的量关系如图,该催化剂在高温时选择反应_____(填“I”或“II”)。
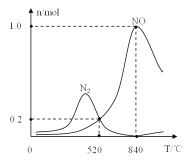
③520℃时,4NH3(g)+3O2 (g)![]() 2N2(g)+6H2O(g)的平衡常数K=_______(只需列出数字计算式)。提高NH3转化为N2平衡转化率的措施有______( 填字母序号)
2N2(g)+6H2O(g)的平衡常数K=_______(只需列出数字计算式)。提高NH3转化为N2平衡转化率的措施有______( 填字母序号)
A.降低反应温度 B.将反应生成的H2O(g)及时移出
C.增大NH3和O2的初始投料比 D.投料比不变,增加反应物的浓度
(3)己知25℃时HCN 和H2CO3的电离常数(Ka.)如下表:
物质 | 电离常数(Ka) |
HCN | Ka=5×10-10 |
H2CO3 | Ka1=4.5×10-7;Ka2=4.7× 10-11 |
25℃时,测得HCN 和NaCN 的混合溶液pH=11,则c(HCN)/c(CN-)=____。向NaCN 溶液中通入少量CO2,则发生反应的离子方程式为:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com