
下列实验中,对应的现象以及结论都正确的是( )
选项 | 实验 | 现象 | 结论 |
A | 向酸性KMnO4溶液中滴加H2O2溶液至过量 | 紫色消失 | H2O2在该反应中作还原剂 |
B | 溶有SO2的BaCl2溶液中通入气体X | 有白色沉淀产生 | X一定是Cl2 |
C | 向FeBr2和KSCN混合溶液中滴入少量现制氯水,再滴入CCl4混合振荡、静置 | 有机相呈红棕色,水相呈无色 | Fe2+的还原性大于Br- |
D | 铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,放入CuSO4溶液中 | 铝丝表明变红色 | 铝可以从铜盐溶液中置换出铜 |
A. A B. B C. C D. D
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源:2017届海南省高三上学期期末化学试卷(解析版) 题型:填空题
已知:环丙烷、环丁烷、环戊烷在催化剂的作用和加热条件下都能与氢气发生类似的反应,如环丁烷与氢气反应可用下列反应式表示: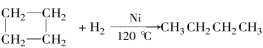
碳原子数不大于4的环烷烃可与卤素、 卤化氢发生类似反应,而碳原子数大于4的环烷烃与卤素则发生取代反应。试填空:
卤化氢发生类似反应,而碳原子数大于4的环烷烃与卤素则发生取代反应。试填空:
(1)环丙烷、环丁烷与Cl2的反应是________(填反应类型);
(2)由环丁烷和Cl2为原料制取1,3-丁二烯的方法是:首先制取_______________________(填结构简式),然后再由它通过_______________________(填反应类型)即得到1,3-丁二烯。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省淮北市高一下学期第一次月考化学试卷(解析版) 题型:填空题
已知下列十种物质:(l) H2O (2) Cu (3) NO (4) Fe2O3 (5)稀硫酸(6)氢氧化钡(7)饱和FeCl3溶液(8)氨水(9)稀硝酸(10)硫酸铝,根据上述提供的物质,回答下列问题:
(1)属于纯净物的是________(填序号),属于电解质的是________(填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为__________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有_____(填序号),反应的离子方程式为____________。
(4)实验室配制245mL 0.5mol/L的硫酸铝溶液,需要称取的溶质的质量为_____g,从配制好的溶液中取出l00mL,其中含有的SO42-的数目为_______(设NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省淮北市高一下学期第一次月考化学试卷(解析版) 题型:选择题
如图是产生和收集气体的实验装置,该装置适合于( )
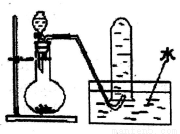
A. 用浓硝酸与Cu反应制取NO2 B. 用浓盐酸和MnO2反应制取Cl2
C. 用H2O2溶液和MnO2反应制取O2 D. 用NH4Cl和Ca (OH)2反应制取NH3
查看答案和解析>>
科目:高中化学 来源:江西省新余市、宜春中学2017届高三下学期开学联考理科综合-化学试卷 题型:简答题
(Ⅰ)甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度℃ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______(用K1、K2表示)。500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15, 则此时 V正_____ V逆(填“ > ”、“=”或“<”)。
(2)在3 L容积可变的密闭容器中发生反应②,已知c(CO)-反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是______________。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是_________________。

(3)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下, 将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为________________。
(Ⅱ)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。
(1)常温下,向10 mL 0.01 mol·L-1 H2C2O4溶液中滴加10mL 0.01mol·L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系_________________________ ;
(2)称取6.0g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解配成250 mL 溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。第一份溶液中加入2滴酚酞试液,滴加0.25mol·L-1 NaOH 溶液至20mL时,溶液由无色变为浅红色。第二份溶液滴加0.10 mol·L-1 酸性KMnO4溶液至16mL时反应完全。则原试样中H2C2O4·2H2O的的质量分数为_______ 。
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三12月月考化学卷(解析版) 题型:实验题
为回收利用废钒催化剂(含有V205、V0S04及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
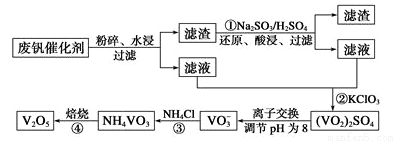
部分含钒物质常温时在水中的溶解性如下:
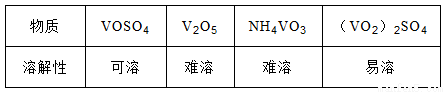
回答下列问题:
(1)废钒催化剂,粉碎的目的是 ,V0S04溶液水解显酸性,离子方程式为
(2)工业上由 V2O5冶炼金属钒常用铝热法,该反应的化学方程式为 引发铝热反应的操作是:在纸漏斗中加入铝热剂后,再
V2O5冶炼金属钒常用铝热法,该反应的化学方程式为 引发铝热反应的操作是:在纸漏斗中加入铝热剂后,再
(3)为了提高钒的浸出率,反应①用Na2SO3和硫酸酸浸使催化剂中的V2O5转变成可溶于水的V0S04,与水浸液合并,再通过反应②用KClO3氧化,使+4价的V氧化成易溶于水的(VO2)2SO4反应①的离子方程式为
(4)该工艺中反应③的沉淀率是回收钒的关键之一,该步反应的离子方程式为 。
(5)已知常温下NH4VO3的溶解度为0.468g/100g水,则NH4VO3的溶度积常数约为 (已知V的相对原子质量为51)。
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三12月月考化学卷(解析版) 题型:选择题
下列试验中,所选装置不合理的是
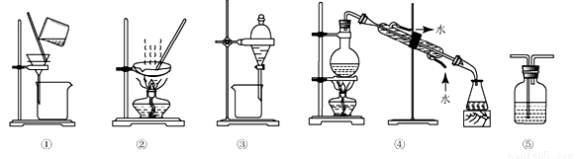
A. 粗盐提纯,选①和②
B. 用CC14提取碘水中的碘,选③
C. 用NaOH溶液吸收少量C12选⑤
D. 分离Na2CO3溶液和CH3COOC2H5,选④
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三第五次模拟化学卷(解析版) 题型:选择题
某溶液中只可能含有下列离子中的某几种:K+、NH4+、Ba2+、SO42-、I-、AlO2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和CCl4振荡后静置,下层呈无色。为确定该溶液的组成,还需检验的离子是
A.K+ B.SO42- C.Ba2+ D.NH4+
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省牡丹江市高三2月开学检测理综化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式不正确的是
A. 向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2=I2+2H2O
B. 在燃煤中加入适量石灰石,可减少SO2的排放:2CaCO3+O2+2SO2═2CaSO3+2CO2
C. 自然界各种原生铜的硫化物经氧化、淋滤作用后产生的硫酸铜,遇到难溶的PbS,慢慢转变为铜蓝(CuS):Cu2++SO42-+PbS═CuS+PbSO4
D. 在盐碱地(含较多NaCl、Na2CO3)上通过施加适量CaSO4,可降低土壤的碱性:CaSO4+Na2CO3═CaCO3↓+Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com