
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2C2O4 | H2S |
电离平衡常数 | 1.8×10﹣5 | Ka1=5.4×10﹣2 | Ka1=1.3×10﹣7 |
请回答下列问题:
(1)H2S的一级电离常数表达式为Ka1=
(2)CH3COOH、H2C2O4、H2S的酸性由强到弱的顺序
(3)H2C2O4与少量的KOH溶液反应的化学方程式:
(4)NaHS溶液与NaHC2O4溶液反应的离子方程式:
(5)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是(填写序号). ①反应所需要的时间B>A
②开始反应时的速率A>B
③参加反应的锌的物质的量A=B
④反应过程的平均速率B>A
⑤B中有锌剩余.
【答案】
(1)Ka1= ![]()
(2)H2C2O4>CH3COOH>H2S
(3)H2C2O4+KOH═KHC2O4+H2O
(4)HS﹣+HC2O4﹣═H2S+C2O42﹣
(5)③④
【解析】解:(1)电离平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比,硫化氢第一步电离平衡常数Ka1= ![]() ,所以答案是:Ka1=
,所以答案是:Ka1= ![]() ;(2)酸的电离平衡常数越大,该酸的酸性越强,CH3COOH、H2C2O4、H2S电离平衡常数大小顺序是,则CH3COOH、H2C2O4、H2S酸性强弱顺序是H2C2O4>CH3COOH>H2S,所以答案是:H2C2O4>CH3COOH>H2S;(3)H2C2O4和少量KOH溶液反应生成草酸氢钾和水,反应方程式为H2C2O4+KOH═KHC2O4+H2O,所以答案是:H2C2O4+KOH═KHC2O4+H2O;(4)NaHS溶液与NaHC2O4溶液生成H2S和草酸钠,离子方程式为HS﹣+HC2O4﹣═H2S+C2O42﹣ , 所以答案是:HS﹣+HC2O4﹣═H2S+C2O42﹣;(5)①反应所需要的时间与反应速率成反比,反应速率与氢离子浓度成正比,反应过程中醋酸继续电离出氢离子,导致氢离子浓度A<B,反应速率A<B,则反应所需时间A>B,故错误;②反应速率与氢离子浓度成正比,开始时A、B氢离子浓度相等,反应速率A=B,故错误;③生成的氢气相同,根据转移电子守恒知,消耗的锌A=B,故正确;④氢离子浓度越大,反应速率越大,反应过程中氢离子浓度A<B,反应过程的平均速率B>A,故正确;⑤酸最终电离出氢离子物质的量越少的,锌可能有剩余,两种酸中酸最终电离出的氢离子浓度A<B,则可能A剩余锌,故错误;故选③④.
;(2)酸的电离平衡常数越大,该酸的酸性越强,CH3COOH、H2C2O4、H2S电离平衡常数大小顺序是,则CH3COOH、H2C2O4、H2S酸性强弱顺序是H2C2O4>CH3COOH>H2S,所以答案是:H2C2O4>CH3COOH>H2S;(3)H2C2O4和少量KOH溶液反应生成草酸氢钾和水,反应方程式为H2C2O4+KOH═KHC2O4+H2O,所以答案是:H2C2O4+KOH═KHC2O4+H2O;(4)NaHS溶液与NaHC2O4溶液生成H2S和草酸钠,离子方程式为HS﹣+HC2O4﹣═H2S+C2O42﹣ , 所以答案是:HS﹣+HC2O4﹣═H2S+C2O42﹣;(5)①反应所需要的时间与反应速率成反比,反应速率与氢离子浓度成正比,反应过程中醋酸继续电离出氢离子,导致氢离子浓度A<B,反应速率A<B,则反应所需时间A>B,故错误;②反应速率与氢离子浓度成正比,开始时A、B氢离子浓度相等,反应速率A=B,故错误;③生成的氢气相同,根据转移电子守恒知,消耗的锌A=B,故正确;④氢离子浓度越大,反应速率越大,反应过程中氢离子浓度A<B,反应过程的平均速率B>A,故正确;⑤酸最终电离出氢离子物质的量越少的,锌可能有剩余,两种酸中酸最终电离出的氢离子浓度A<B,则可能A剩余锌,故错误;故选③④.
【考点精析】本题主要考查了弱电解质在水溶液中的电离平衡的相关知识点,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理才能正确解答此题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】X,Y,Z三种物质中含同种元素,在一定条件下可以实现如图所示转化,下列推断不正确的是( ) 
A.若Y为氧化铝,则Y 生成X的条件是“通电”
B.若X为硫单质,则Y 可能为硫化氢
C.若Z为硝酸,则X可能为一氧化氮
D.若Z为硝酸铁,则Y一定为铁单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是( )

A. Mg2+、Al3+、Ba2+ B. H+、Mg2+、Al3+
C. H+、Cu2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取.以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI+3H2O ![]() KIO3+3H2↑.下列有关说法正确的是( )
KIO3+3H2↑.下列有关说法正确的是( )
A.电解时,石墨作阴极,不锈钢作阳极
B.电解时,阳极反应是:I﹣﹣6e﹣+3H2O=IO3﹣+6H+
C.溶液调节至强酸性,对生产有利
D.电解前后溶液的pH几乎不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是( )
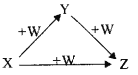
①Na、Na2O、Na2O2 ②AlCl3、Al(OH)3、NaAlO2 ③Fe、FeCl2、FeCl3 ④NaOH、Na2CO3、NaHCO3 ⑤C、CO、CO2
A. ①②③④⑤ B. ②④ C. ①③⑤ D. ①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等.化学在解决雾霾污染中有着重要的作用.
(1)已知:2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol ﹣12NO(g)+O2(g)2NO2(g)△H=﹣113.0kJmol﹣1
则反应NO2(g)+SO2(g)SO3(g)+NO(g)△H=kJmol﹣1 .
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K= .
(2)如图1是一种用NH3脱除烟气中NO的原理. 
①该脱硝原理中,NO最终转化为H2O和(填化学式).
②当消耗1mol NH3和0.5molO2时,除去的NO在标准状况下的体积为L.
(3)NO直接催化分解(生成N2和O2)也是一种脱硝途径.在不同条件下,NO的分解产物不同.在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图2所示,写出NO分解的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D是由常见的短周期非金属元素形成的单质,常温下A是淡黄色粉末,B、D是气体,F、G、H的焰色反应均为黄色,水溶液均显碱性,E有漂白性。它们之间的转化关系如图所示(部分产物及反应条件已略去),回答下列问题:
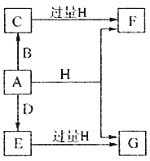
(1)A所含元素在周期表中的位置为______________,C的电子式为_______________。
(2)A与H在加热条件下反应的化学方程式为__________________。
(3)将A溶于沸腾的G溶液中可以制得化合物I,I在酸性溶液中不稳定,易生成等物质的量的A和E,I在酸性条件下生成A和E的离子方程式为____________________。I是中强还原剂,在纺织、造纸工业中作为脱氯剂,向I溶液中通入氯气可发生反应,参加反应的I和氯气的物质的量比为1:4,该反应的离子方程式为__________________。
(4)向含有0.4molF、0.1molG的混合溶液中加入过量盐酸,完全反应后收集到aL气体C(标准状况),取反应后澄清溶液,加入过量FeCl3溶液,得到沉淀3.2g,则a=____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.01molL﹣1HA溶液中逐滴加入0.02molL﹣1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题: 
(1)由图中信息可知HA为酸(填“强”或“弱”),理由是
(2)常温下一定浓度的MA稀溶液的pH=a,则a7(填“>”、“<”或“=”),用离子方程式表示其原因为;,此时,溶液中由水电离出的c(OH﹣)= .
(3)请写出K点所对应的溶液中离子浓度的大小关系:
(4)K点对应的溶液中,c(M+)+c(MOH)2c(A﹣)(填“>”、“<”或“=”);若此时溶液中,pH=10,则c(MOH)+c(OH﹣)=molL﹣1 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com