
一种熔融碳酸盐燃料电池原理示意如图,下列有关该电池的说法正确的是( )
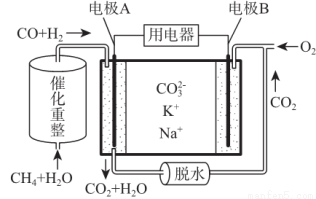
A.反应CH4+H2O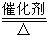 3H2+CO,每消耗1molCH4转移6mol电子
3H2+CO,每消耗1molCH4转移6mol电子
B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C.电池工作时,CO32-向电极B移动
D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
科目:高中化学 来源:2015-2016学年江苏省高一下期中化学试卷(解析版) 题型:选择题
某原电池的总反应式是Zn +Cu2+=Zn2+ + Cu,该反应的原电池的正确组成是
选项 | A | B | C | D |
正极材料 | Zn | C | Zn | Mg |
负极材料 | Cu | Zn | Ag | Zn |
电解质溶液 | CuCl2 | CuSO4 | CuSO4 | CuCl2 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
Li﹣Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e﹣=Li2S+Fe。有关该电池的下列说法中,正确的是
A.Li﹣Al在电池中作为负极材料,该材料中Li的化合价为+1价
B.该电池的电池反应式为:2Li+FeS=Li2S+Fe
C.负极的电极反应式为Al﹣3e﹣=Al3+
D.充电时,阴极发生的电极反应式为:Li2S+Fe﹣2e﹣=2Li++FeS
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三高考考前模拟十二化学试卷(解析版) 题型:选择题
根据如图海水综合利用的工业流程图,判断下列说法正确的是( )
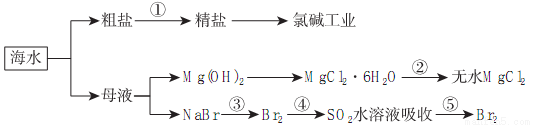
A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.在过程④中SO2被氧化
C.从第③步到第⑤步的目的是为了浓缩
D.从能量转换角度看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三高考考前模拟十二化学试卷(解析版) 题型:填空题
已知有关热化学方程式为:①4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g)
4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g) 2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反应①中有关化学键的键能(kJ/mol)如下:H—O:463,H—N:391,O=O:497
2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反应①中有关化学键的键能(kJ/mol)如下:H—O:463,H—N:391,O=O:497
(1)①Q=___________。
②NO中的化学键键能为_________kJ/mol。
(2)向某密闭容器中充入amolNH3、bmolO2后,测得反应体系中某种量值X与压强P、温度T之间的变化如图1所示,图2表示温度为T2时,当容器为1L恒容密闭容器时,容器中NH3的平衡转化率与反应开始时两种反应物的投料之比(用M表示)的关系。
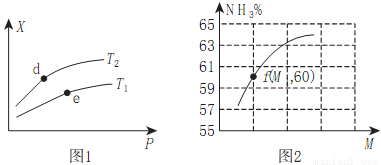
①若X表示NH3的百分含量,则T2_____T1(填>、<、无法确定);d、e两点的正反应的平衡常数K(d)_____K(e)。
②X还可以表示_____________。
A.混合气体的平均摩尔质量B.NO的产率C.△H值
③M=__________(用含a、b的式子表示,后同),若M1=1.25,则此时O2的转化率为__________%。
(3)有科学家电解原理获得高产率的合成氨,则阴极上的电极反应式为(已知电解质能传递H+)_______________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三高考考前模拟十二化学试卷(解析版) 题型:选择题
相对分子质量为86的某烃M,其分子中含有4个甲基,则A的一氯代物(不考虑立体异构)最多有( )
A.6种 B.5种 C.4种 D.3种
查看答案和解析>>
科目:高中化学 来源:2016届江西省、临川二中高三下联考理综化学试卷(解析版) 题型:简答题
以下是某企业设计的硫酸——磷肥——水泥联产、海水——淡水多用、盐——热——电联产的三大生态产业链流程图。根据上述产业流程回答下列问题:

(1)该流程①、③、④为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:①________ ③________ ④________
(2)沸腾炉发生反应的化学方程式为: ,磷肥厂的主要产品是普钙(磷酸二氢钙和硫酸钙),写出由磷矿石和硫酸反应制普钙的化学方程式:
(3)用1吨硫铁矿(FeS2的质量分数为36%)接触法制硫酸,制硫酸的产率为65%,则最后能生产出质量分数为98%的硫酸________吨。
(4)热电厂的冷却水是海水,该流程中浓缩盐水中含有K+、Na+、Mg2+等阳离子,对母液进行一系列的加工可制得金属镁。
①从离子的反应的角度思考,在浓缩盐水中加入石灰乳所起的作用是_____________。
②要利用MgCl2·6H2O制得无水氯化镁,应采取的措施是_________________________。
③电解熔融的无水氯化镁所得的镁蒸气在特定的环境中冷却后即为固体镁。下列物质中可以用作镁蒸气冷却剂的是________(填选项字母)
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
(5)炼铁过程中加入 除去废渣中的含硅杂质。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三下学期周考五理科综合化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、R的原子序数依次增大,核电荷数之和为36;X、Z原子的最外层电子数之和等于Y原子的次外层电子数;R原子的质子数是Y原子质子数的两倍.下列有关这四种元素的相关叙述正确的是( )
A.X与Z组成的化合物溶于水呈碱性
B.只有Y元素存在同素异形体
C.R的氢化物比Y的氢化物的沸点更高
D.X、Y、Z、R形成简单离子的半径依次增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁鞍山一中高二下期中化学试卷(解析版) 题型:选择题
以下几句话中不正确的有( ) 句
①晶体在受热熔化过程中一定存在化学键的断裂
②卤化氢易溶于水,不易溶于四氯化碳
③NaCl晶体中与每个Na+距离相等且最近的Na共有8个
④固体分子中一定存在分子间作用力,不一定存在化学键
⑤HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强
⑥F2、Cl2、Br2、I2的沸点依次升高
⑦金属Mg晶体中,Mg原子的配位数为12; CsCl晶体中阴、阳离子的配位数都为6
⑧乳酸(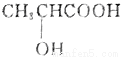 )有一对手性异构体,因为其分子中含有一个手性碳原子
)有一对手性异构体,因为其分子中含有一个手性碳原子
A.1句 B.2句 C.3句 D.4句
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com