
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴甲基橙 | 溶液变红色 |
| (2)取少量该溶液加热浓缩,加Cu片和浓硫酸,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| (4)取少量该溶液,加AgNO3 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| (5)取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化钠溶于水中 |
| B、NH3 (g)和HCl(g)反应生成NH4Cl |
| C、干冰的升华 |
| D、CaCO3 (S)分解为CaO(S)和CO2 (g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.25molSO3 |
| B、0.5molCO2 |
| C、1mol氖气 |
| D、1molCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuSO4?5H2O、冰、乙醇 |
| B、KCl、氢氧化铁胶体、NaOH |
| C、金刚石、干冰、SO2 |
| D、臭氧、CaCO3、铝合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| | 操作和现象 | 结论 |
| A | 取某溶液少许,加入盐酸酸化的BaCl2溶液,出现白色沉淀 | 该溶液中一定含有SO42- |
| B | 向纯碱溶液中滴加足量稀盐酸,将产生的气体通入苯酚钠溶液中,溶液变浑浊 | 酸性:盐酸>碳酸>苯酚 |
| C | 某溶液中加入盐酸产生能使澄清石灰水变浑浊的气体 | 该溶液一定含有CO32-或SO32- |
| D | 取少量Fe(NO3)2试样加稀硫酸溶解,滴加KSCN溶液,溶液变红色 | 该Fe(NO3)2试样已经变质 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丙炔 | B、1-丁炔 | C、丁烯 | D、苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
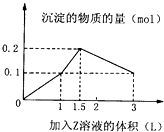 某1L混合溶液中,溶质X、Y的浓度都为0.1mol?L-1,向混合溶液中滴加某溶液Z(0.1molL-1氢氧化钠或硫酸溶液),所得沉淀的物质的量如图所示,则X、Y、Z分别是( )
某1L混合溶液中,溶质X、Y的浓度都为0.1mol?L-1,向混合溶液中滴加某溶液Z(0.1molL-1氢氧化钠或硫酸溶液),所得沉淀的物质的量如图所示,则X、Y、Z分别是( )| A、硫酸铝、硫酸铁、氢氧化钠 |
| B、硫酸铝、硫酸镁、氢氧化钠 |
| C、偏铝酸钠、氢氧化钡、硫酸 |
| D、偏铝酸钠、氯化钡、硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com