
【题目】在反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O 中
(1)用单线桥标出电子转移
(2)还原剂是 , 被还原的元素是 , 还原产物是 .
(3)若生成2mol的NO气体,溶液中生成的Cu2+为mol.
(4)在反应中硝酸显示性和性.
【答案】
(1)![]() =3Cu(NO3)2+2NO↑+4H2O
=3Cu(NO3)2+2NO↑+4H2O
(2)Cu; N; NO
(3)3
(4)酸;氧化
【解析】解:(1)该反应中铜元素的化合价变化为0价→+2价,氮元素的化合价变化为+5价→+4价,所以得失电子的最小公倍数是2,所以其电子转移的方向和数目为 ![]() =3Cu(NO3)2+2NO↑+4H2O,
=3Cu(NO3)2+2NO↑+4H2O,
所以答案是: ![]() =3Cu(NO3)2+2NO↑+4H2O;(2)铜元素的化合价升高,Cu是还原剂,氮元素的化合价降低,硝酸被还原,NO为还原产物;
=3Cu(NO3)2+2NO↑+4H2O;(2)铜元素的化合价升高,Cu是还原剂,氮元素的化合价降低,硝酸被还原,NO为还原产物;
所以答案是:Cu;N;NO;(3)3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O中,若生成2mol的NO气体,溶液中生成的Cu2+为3mol;
所以答案是:3;(4)N元素的化合价降低,则HNO3为氧化剂,硝酸表现氧化性,反应生成硝酸铜,硝酸表现酸性;
所以答案是:酸;氧化.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
【题目】验证NH4Cl晶体中含有NH4+ . 将少量晶体于两端开口的硬质玻璃管中加热,如图所示. 
(1)氯化铵受热反应的化学方程式是 .
(2)检验氨气时,可在处(填“a”或“b”)用湿润试纸,现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组同学查阅文献,并用图装置进行实验. ⅠSO2不能与BaCl2反应;ⅡBaSO3是白色难溶于水的物质,但可溶解于盐酸.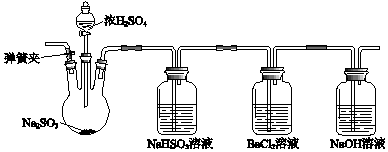
(1)该实验制备SO2的化学方程式是 .
(2)BaCl2溶液中出现了不溶于稀盐酸的白色沉淀,该沉淀可能是 .
(3)甲同学认为出现白色沉淀是由于装置中存在O2 , 排除干扰的方法是 .
(4)按照(3)中改进后的方法重新进行实验,现象是 , 实验结论与文献一致.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理知识研究如何利用CO、SO2等污染物有重要意义.
(1)用CO可以合成甲醇.已知:
CH3OH(g)+ ![]() O2(g)═CO2(g)+2H2O(l)△H 1 kJmol﹣1
O2(g)═CO2(g)+2H2O(l)△H 1 kJmol﹣1
CO(g)+ ![]() O2(g)═CO2(g)△H2 kJmol﹣1
O2(g)═CO2(g)△H2 kJmol﹣1
H2(g)+ ![]() O2(g)═H2O(l)△H3 kJmol﹣1
O2(g)═H2O(l)△H3 kJmol﹣1
则CO(g)+2H2(g)CH3OH(g)△H=kJmol﹣1 .
(2)一定压强下,在容积为2L的密闭容器中充入1mol CO与2mol H2 , 在催化剂作用下发生反应:CO(g)+2H2(g) CH3OH(g)△H,平衡转化率与温度、压强的关系如图1所示. 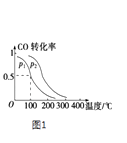
①下列说法正确的是
A.若容器内气体密度恒定,反应达到平衡状态
B.若容器内各气体浓度恒定,反应达到平衡状态
C.上述反应中,△H>0
D.反应中,催化剂使平衡向正反应方向移动
②p2p1 (填“大于”、“小于”或“等于”);
③100℃时,该反应的化学平衡常数K=;
(3)某科研小组用SO2为原料制取硫酸.
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触.请写出该电池负极的电极反应式: .
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸.电解原理示意如图2所示.请写出开始时阳极反应的电极反应式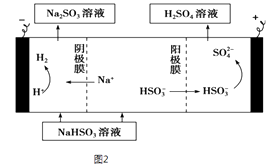
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些化学反应可用下式表示:A+B→C+D+H2O请回答下列问题:
(1)若A,C,D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式: .
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,则A与B的组合是:或 .
(3)若A为MnO2 , B为盐酸,C是黄绿色的单质气体,写出该反应的离子方程 式 .
(4)若A为单质,B为硝酸,请写出符合上式的化学方程式 .
(5)若C、D均为气体且都能使澄清石灰水变浑浊,且D可以使品红褪色,则A与B反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的好似( )
A.已知2H2O(l)═2H2(g)+O2(g)△H=+571.6KJmol﹣1 , 无法求H2的燃烧热
B.已知C(石墨,s)=C(金刚石,s)△H>0,无法比较二者的稳定性
C.已知500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放出19.3KJ的热量,无法推出该反应的热化学方程式
D.已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2 , 无法得出△H2>△H1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁是一种很重要的铁盐,有广泛的用途,可用于金属蚀刻,污水处理,印染滚筒刻花,电子工业线路板及荧光数字筒生产等.该化合物呈棕红色、易潮解,100℃左右时升华,某实验小组组合一下实验装置来制备纯净的氯化铁.试回答: 
(1)仪器A的名称: .
(2)实验装置正确的连接顺序:I接、、、接Ⅱ;其中装置Ⅲ和Ⅴ的作用分别是和 .
(3)如何检查整个装置的气密性: .
(4)装置Ⅳ两试剂瓶中的试剂分别是和(填名称).
(5)装置Ⅱ中反应化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面4组物质中,能发生反应且既属于离子反应又属于氧化还原反应的是( )
A. 硫酸钠溶液与氯化钡溶液 B. 铝片与硝酸汞溶液
C. 稀硫酸与铜片 D. 硝酸钠溶液与氯化钾溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com