
| A�� | 3��3-����-1-��ϩ�������õ�3��3-����-���� | |
| B�� | 2-��-1��3-����ϩ��Br2�ļӳɲ�����3�� | |
| C�� | ��������ԭ�Ӳ���ͬһƽ���Ͽ���˵��C4H6��ij����1-��Ȳ������CH2=CH-CH=CH2 | |
| D�� | ��֪���е�˫�����泤�����磺-CH=CH-CH=CH-CH=CH-���ĸ߷����п��ܳ�Ϊ�������ϣ��ʾ���ϩ�;���Ȳ���ɳ�Ϊ�������� |
���� A���ȸ��ݼӳ�ԭ���������ͼ��Ͽ������Hԭ�ӣ�Ȼ���������������ԭ����������жϣ�
B��2-��-1��3-����ϩ�ṹ��ʽΪCH2=C��CH3��CH=CH2���������巢���ӳɷ�Ӧ��������1��2-�ӳɡ�������3��4-�ӳɣ�Ҳ������1��4-�ӳɣ�Ҳ������1��2��3��4-�ӳɣ�
C������1-��Ȳ��1��3-����ϩƽ��ṹ���з�����
D��������֪���е�˫�����泤������һCH=CH-CH=CH-CH=CHһ���ĸ߷����п��ܳ�Ϊ�������ϣ�
��� �⣺A��3��3-����-1-��ϩ��CH2=CH-C��CH3��3�����������ӳɷ�Ӧ����������CH3-CH2-C��CH3��3����������������ԭ��ѡȡ��̼���Ϊ��̼��Ϊ4��̼ԭ�ӣ�����Ϊ֧��������֧������һ�˱������ȷ��֧��λ�ã�����Ҫ��д������Ϊ2��2-�������飬��A����
B��2-��-1��3-����ϩ�ṹ��ʽΪCH2=C��CH3��CH=CH2���������巢���ӳɷ�Ӧ��������1��2-�ӳɡ�������3��4-�ӳɣ�Ҳ������1��4-�ӳɣ�Ҳ������1��2��3��4-�ӳɣ�������ӳɲ�����4�֣���B����
C��1��3-����ϩ������ԭ�Ӷ���ͬһƽ���ϣ���1-��Ȳ������3��4̼ԭ���ϵ���ԭ�Ӳ���ͬһƽ���ϣ���C��ȷ��
D�����е�˫�����泤������һCH=CH-CH=CH-CH=CHһ���ĸ߷����п��ܳ�Ϊ�������ϣ�����ϩ�ж�ֻ���е��������ɳ�Ϊ�������ϣ�������Ȳ���ǵ�˫������Ľṹ���ɳ�Ϊ�������ϣ���D����
��ѡC��
���� ���⿼���л���ṹ�������Լ���������ȷ��ϩ�������ӳ��ص��ǽⱾ��ؼ���ע�ⲻ��©���ӳ������Ϊ�״��⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
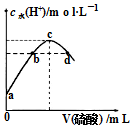 �����£���20mL0.1mol•L-1��ˮ�еμ�ijŨ�ȵ�������Һ����Һ��ˮ�����������Ũ����������������仯��ͼ������˵��������ǣ�������
�����£���20mL0.1mol•L-1��ˮ�еμ�ijŨ�ȵ�������Һ����Һ��ˮ�����������Ũ����������������仯��ͼ������˵��������ǣ�������| A�� | ��a����1.0��10-11 mol•L-1�����ʱ��ˮ�ĵ����Ϊ1% | |
| B�� | c��ʱ��ˮ������ǡ����ȫ��Ӧ | |
| C�� | c����ʾ��Һ�У�c��H+��-c��OH-���Tc��NH3•H2O�� | |
| D�� | ��b��d��Ӧ��ˮ�����������Ũ��Ϊ1.0��10-7 mol•L-1����ʱ����Һ�ж����ڣ�c��NH4+���T2c��SO42-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
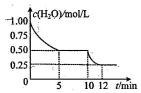 ��2L�ܱ������н��з�ӦC��s��+H2O��g��?CO��g��+H2��g����H��0�����c��H2O���淴Ӧʱ�䣨t���ı仯��ͼ�������ж���ȷ�ǣ�������
��2L�ܱ������н��з�ӦC��s��+H2O��g��?CO��g��+H2��g����H��0�����c��H2O���淴Ӧʱ�䣨t���ı仯��ͼ�������ж���ȷ�ǣ�������| A�� | 0��5min�ڣ�v��H2��=0.05mol/��L•min�� | |
| B�� | 5minʱ�÷�Ӧ��Kֵһ��С��12minʱ��Kֵ | |
| C�� | 10minʱ���ı��������������Ǽ�Сѹǿ | |
| D�� | 5minʱ�÷�Ӧ��v����������11minʱ��v���棩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
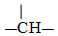 ��
�� �Ƚ�϶��ɵģ���д��ͬʱ�������������������Ľṹ��ʽ��
�Ƚ�϶��ɵģ���д��ͬʱ�������������������Ľṹ��ʽ��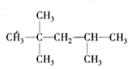
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ | B�� | �Ҵ������ᣩ | C�� | �������������ᣩ | D�� | ���ᣨ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3g ${\;}_{1}^{3}$H�����˷�Ӧ��${\;}_{1}^{2}H$+${\;}_{1}^{3}H$��${\;}_{2}^{4}He$+${\;}_{0}^{1}n$����������������ΪNA | |
| B�� | 0.1L1mol/L���Ậ�е�H+����ĿΪ0.1NA | |
| C�� | ��״���£�22.4LCCl4���е�ԭ����ĿΪ5 NA | |
| D�� | 1L0.4mol/LŨ������������MnO2��Ӧת�Ƶ��ӵ����ʵ���Ϊ0.2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
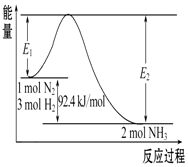 ��ѧ��һֱ�����ڡ��˹��̵����ķ����о���
��ѧ��һֱ�����ڡ��˹��̵����ķ����о���| t�� | 473 | 573 | 673 | �� |
| K | 4.4��10-2 | K1 | K2 | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com