
原子序数为83的元素位于:①第5周期;②第6周期;③ⅣA族;④ⅤA族;⑤ⅡB族,其中正确的组合是( )
A.①④ B.②③ C.②④ D.①⑤
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
某溶液可能含有Na+、Ag+、Al3+、S2-、CO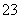 、SO
、SO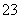 、NO
、NO 等离子中的数种。向此溶液中加入稀盐酸,有浅黄色沉淀和气体出现,此溶液的焰色为黄色。根据以上实验现象,下列关于原溶液中离子成分的推测正确的是( )
等离子中的数种。向此溶液中加入稀盐酸,有浅黄色沉淀和气体出现,此溶液的焰色为黄色。根据以上实验现象,下列关于原溶液中离子成分的推测正确的是( )
A.一定有S2-、SO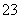 、Na+
、Na+
B.可能只有Na+、S2-、CO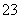
C.一定没有Ag+、Al3+
D.一定有Na+、S2-、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
Nomex纤维是一种新型阻燃纤维,其结构简式为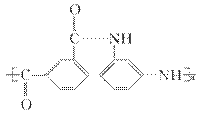 ,据此可以推知在一定条件下,以等物质的量发生缩聚反应生成该物质的两种单体是( )。
,据此可以推知在一定条件下,以等物质的量发生缩聚反应生成该物质的两种单体是( )。
A.间苯二甲酸和邻苯二胺
B.间苯二甲酸和间苯二胺
C.间苯二甲酸和对苯二胺
D.对苯二甲酸和对苯二胺
查看答案和解析>>
科目:高中化学 来源: 题型:
可以由下列反应合成三聚氰胺:CaO+3C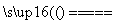 CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2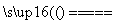 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_____________________________________________。
CaCN2中阴离子为CN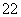 ,与CN
,与CN 互为等电子体的分子有N2O和________(填化学式),由此可以推知CN
互为等电子体的分子有N2O和________(填化学式),由此可以推知CN 的空间构型为________。
的空间构型为________。
(2)尿素分子中C原子采取________杂化。尿素分子的结构简式是________。
 (3)三聚氰胺(
(3)三聚氰胺(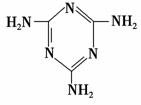 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(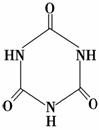 )后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
)后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
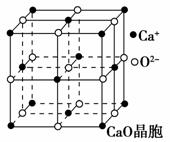
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________。CaO晶体和NaCl晶体的晶格能分别为:CaO 3 401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是__________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.周期表中的主族都有非金属元素
B.周期表中的主族都有金属元素
C.周期表中的非金属元素都位于短周期
D.周期表中的过渡元素都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F代表6种元素。请填空:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为__________。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为________,C的元素符号为________。
(3)D元素的正三价离子的3d轨道为半充满,D的元素符号为________,其基态原子的电子排布式为_________________________________________________________________。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为________,其基态原子的电子排布式为__________________________________。
(5)F元素的原子最外层电子排布式为nsnnpn+1,则n=________;原子中能量最高的是________电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
四种元素中的第一电离能最小的是__________,电负性最大的是__________。(填元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是( )
①CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=890.3 kJ·mol-1
②CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=-890.3 kJ·mol-1
③CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-890.3 kJ·mol-1
④2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6 kJ·mol-1
A.仅有② B.仅有②④ C.仅有②③④ D.全部符合要求
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com