


 �ŵ������ϵ�д�
�ŵ������ϵ�д� 53������ϵ�д�
53������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��BaSO4��BaCO3�ܽ��С�����ԣ�BaCO3������ת��ΪBaSO4 | ||
| B��BaCO3��BaSO4��������ˮ�����Զ������������Լ� | ||
C���κ��¶��£���Na2CO3��Һ�м���BaCl2��Na2SO4�������ֳ�������ʱ��
| ||
| D�����¶��£�BaCO3��Ҫ��Na2SO4��Һ��ת��ΪBaSO4����Na2SO4Ũ������Ϊ2.2��10-6mol?L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ���Լ� | ʵ������ | |
| ��һ�ַ��� | ||
| �ڶ��ַ��� |
| ʵ�鲽�� | ʵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
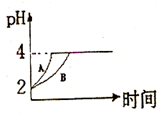 ѡ����ģ���ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺
ѡ����ģ���ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
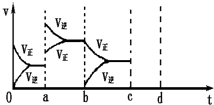 ��1����ͼ��ʾ���ܱ������з�Ӧ��2SO2+O2?2SO3��H��0�ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����ab�����иı������������
��1����ͼ��ʾ���ܱ������з�Ӧ��2SO2+O2?2SO3��H��0�ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����ab�����иı������������| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH3COONa |
| B��AlCl3 |
| C��NaHCO3 |
| D��Ba��NO3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol/L NH4Cl��Һ��c��NH4+ ��=c��Cl-�� |
| B��0.1mol/L NaHCO3��Һ��c��OH-��+c��CO32-��=c��H+��+c��H2CO3�� |
| C��0.3mol/L��0.1mol/L����������Һ��H+����Ũ��֮��Ϊ3��1 |
| D��25��ʱ��pH=4.75��Ũ�Ⱦ�Ϊ0.1mol?L-1��CH3COOH��CH3COONa�����Һ��c��CH3COO-��+c��OH-����c��CH3COOH��+c��H+�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com