
����Ŀ��һ���¶��£����ݻ�ΪV L���ܱ������н��з�Ӧ��M��N������������ʵ�����ʱ��ı仯������ͼ��ʾ��
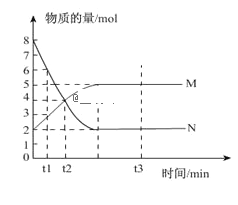
(1)�÷�Ӧ����������___________��
(2)�÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ_____________��
(3)��t2ʱ�̣���M��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ____________��
(4)���ﵽƽ��״̬��ʱ����4 min��N�����ڸ�4 min�ڵ�ƽ����Ӧ����Ϊ1.5mol��L-1��min-1������������ݻ�V=____________L��
(5)�ﵽƽ��״̬ʱ����Ӧ���ת����Ϊ____________��
���𰸡�M 2NM 2/(V��t2) mol/(L��min) 1 75%
��������
(1)���ŷ�Ӧ��������Ӧ��������ϼ�С������������������ӽ����ж���
(2)����ʽ�и����ʵ�ϵ���Ⱥ����ʳ��������ݴ�д���÷�Ӧ����ʽ��
(3)����v=c/t�������
(4)����v=c/t=n/Vt�������
(5)����ת����=N�ı仯��/N��ʼ����100%���м�����
(1)��ͼ�����֪��,���ŷ�Ӧ������N�����ʵ�������,M�����ʵ�������,����N�Ƿ�Ӧ��,M����������
��ˣ�������ȷ����: M ��
(2)��Ӧ���е�ijһʱ�������Ӧ��N�����ʵ���Ϊ��ֵ�Ҳ�Ϊ��,���Ը÷�ӦΪ���淴Ӧ,��n(N): n(M)=(8-2)����5-2��=2:1,��Ӧ�Ļ�ѧ����ʽΪ:2N![]() M��
M��
��ˣ�������ȷ����:2N![]() M��
M��
(3) ��t2ʱ�̣���M��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊv=c/t=[(4-2)/V ]/ t2=2/(V��t2) mol/(L��min)��
�������������������2/(V��t2) mol/(L��min)��
(4)���ﵽƽ��״̬��ʱ����4 min��N�����ڸ�4 min�ڵ�ƽ����Ӧ����Ϊ1.5mol��L-1��min-1��N�ı仯��Ϊ1.5��4��Vmol������ͼ���֪��1.5��4��V=8-2=6��V=1L��
�������������������1��
(5)�ﵽƽ��״̬ʱ������ͼ���֪��Ӧ��N�ı仯��Ϊ8-2=6mol��Nת����Ϊ6/8��100%=75%��
�������������������75%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӵ�ʳ���к��е����(KIO3)�����Ե�ⷨ�Ʊ�����أ�ʵ��װ����ͼ��ʾ���Ƚ�һ�����ĵ����ڹ�������������Һ��������Ӧ��3I2��6KOH===5KI��KIO3��3H2O��������Һ��������������������������Һ��������������ʼ��⡣����˵������ȷ����(����)

A. ��������OH����a����ͨ�����ӽ���Ĥc����b����
B. ���ŵ����У�KOH��ҺŨ�Ȼ���С
C. a�缫��Ӧʽ��I����6e����6OH��=== IO![]() ��3H2O��a������KI����ת��ΪKIO3
��3H2O��a������KI����ת��ΪKIO3
D. ��������0.1 mol I���ŵ�ʱ����������6.72 L H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���γɻ�������������Ԫ�أ��䵥�ʼ������������������������Ҫ��Դ���ʡ�
(1)�л���M����̫������տ�ת����N��ת���������£�
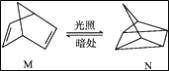 ��H=+88.6 kJ��mol��1
��H=+88.6 kJ��mol��1
��M��N��ȣ����ȶ�����__________��
(2)���������Ȼ�ѧ����ʽ������C��s����ȼ���ȡ�H����_____________ ���á�H1 ����H2����H3��ʾ��
C��s��+H2O��l��=CO��g��+H2��g���� ��H1
2CO��g��+O2��g��=2CO2��g���� ��H2
2H2��g��+O2��g��=2H2O��l���� ��H3
(3) ���ݼ������ݹ���CH4(g)��4F2(g)===CF4(g)��4HF(g)�ķ�Ӧ�Ȧ�H��________��
��ѧ�� | C��H | C��F | H��F | F��F |
����/(kJ��mol��1) | 414 | 489 | 565 | 155 |
CH4�Ľṹ��ͼ��ʾ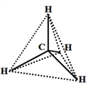
(4)ʹCl2��H2O(g)ͨ�����ȵ�̿�㣬����HCl��CO2������1 mol Cl2���뷴Ӧʱ�ͷų�145 kJ������д���÷�Ӧ���Ȼ�ѧ����ʽ��____________________________��
(5)��ʯī�����ۺͶ������Ѱ�һ����������ڸ��������գ��������ʿ������²��ϣ�4Al(s)+3TiO2(s)+3C(s) =2Al2O3(s)+3TiC(s) ��H= ��1176 kJ��mol��1����Ӧ�����У�ÿת��1 mol���ӷų�������Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ 2NO2(g)![]() N2O4(g) ��H<0, ����ѹǿ,����˵����ȷ����(����)
N2O4(g) ��H<0, ����ѹǿ,����˵����ȷ����(����)
A. ƽ�������ƶ� B. ���������ɫ��ԭ����
C. ���������ɫ��ԭ��dz D. ��������ƽ����Է���������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ڲ��Ϸ����Ӧ��Խ��Խ�㷺��
(1)�װ�(CH3NH2)�Ǻϳ�̫������������ԭ�ϡ���ҵ�ϳɼװ�ԭ����
CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g)��H��
CH3NH2(g)+H2O(g)��H��
����֪����ָ�Ͽ�1mol��̬�������յ��������γ�1mol��̬�����ͷŵ����������ֻ�ѧ���ļ������±���ʾ��
��ѧ�� | C-H | C-O | H-O | N-H | C-N |
����/kJ��mol-1 | 413 | 351 | 463 | 393 | 293 |
��úϳɷ�Ӧ�ġ�H=______________��
��һ�������£��������ͬ�ļס��ҡ��������ĸ������У���ʼͶ���������£�
NH3(g)/mol | CH3OH(g)/mol | ��Ӧ���� | |
�� | 1 | 1 | 498K������ |
�� | 1 | 1 | 598K������ |
�� | 1 | 1 | 598K����ѹ |
�� | 2 | 3 | 598K������ |
�ﵽƽ��ʱ���ס��ҡ������������е�CH3OHת�����ɴ�С��˳��Ϊ_______________��
(2)��ҵ��������(Ga)��NH3�ڸ����ºϳɹ���뵼����ϵ�����(GaN)���䷴Ӧԭ��Ϊ2Ga(s)+2NH3(g)![]() 2GaN(s)+3H2(g)��H=-30.81kJ��mol-1��
2GaN(s)+3H2(g)��H=-30.81kJ��mol-1��
�����ܱ������г���һ������Ga��NH3������Ӧ��ʵ���÷�Ӧ��ϵ���¶ȡ�ѹǿ�����������ͼ��ʾ��ͼ��A����C��Ļ�ѧƽ�ⳣ���ֱ�ΪKA��KC,���й�ϵ��ȷ����_________(�����)��
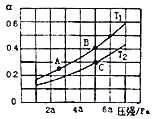
a������a��ʾNH3��ת���� b������a��ʾNH3��������� c��T1<T2 d��KA<Kc
������Ԫ�����ڱ�λ�ڵ������ڵڢ�A�壬��ѧ�����������ơ������������ȶ���������ˮ�����ܻ����ܽ����ȵ�NaOH��Һ�У��÷�Ӧ�����ӷ���ʽΪ_____________________��
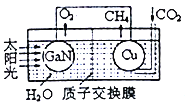
(3)�õ�������ͭ�����ͼ��ʾ���˹����ϵͳ�����ø�װ�óɹ�����CO2��H2OΪԭ�Ϻϳ�CH4��ͭ�缫���淢���ĵ缫��ӦʽΪ___________�����缫�ų�O2��CH4��ͬ�����µ������Ϊ________��Ϊ��߸��˹����ϵͳ�Ĺ���Ч�ʣ�����װ���м���������__________(����ᡱ�����ᡱ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��X��Y��Z��Q�����ڱ��е�λ����ͼ��ʾ������Ԫ��Qλ�ڵ������ڣ�X��Y��Zԭ�ӵ�����������֮��Ϊ17������˵����ȷ����
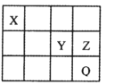
A. �����Ӱ뾶(r)��r(Q)>r(Y)>r(Z)
B. �������Ӧ��ˮ��������ԣ�Z>Y
C. XY2��XZ4�����зǼ��Թ��ۼ�
D. ��״����Z�ĵ���״̬��Q����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���軯��(NaCN)��һ�ֻ�������ԭ�ϣ�ͬʱҲ��һ�־綾���ʡ�һ��й©��Ҫ��ʱ������һ�����ͨ������˫��ˮ��������ƣ�Na2S2O8����Һ���������Լ��ỷ����Ⱦ��
I.(1)NaCN��˫��ˮ��������һ����ʽ�κ�һ����ʹʪ��ĺ�ɫʯ����ֽ���������壬�÷�Ӧ�Ļ�ѧ����ʽ��____________________��
��.��ҵ�Ʊ��������Ƶķ�Ӧԭ�����£�
����Ӧ![]()
����Ӧ��![]()
ij��ѧС����������ԭ����ʵ�����Ʊ��������ƣ����ù���������Һ�������軯�Ƶķ�ˮ��
ʵ��һ��ʵ����ͨ������ͼ��ʾװ���Ʊ�Na2S2O8��
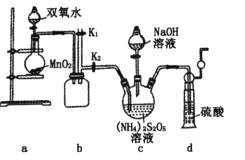
(2)װ����ʢ��˫��ˮ������������_________��
(3)װ��a�з�Ӧ������������Ҫ����ͨ��װ��c��ԭ����______________________��
(4)����װ���л��貹���ʵ��������װ����__________(����ĸ)��
A.�¶ȼ� B.ϴ��ƿ C.ˮԡ����װ�� D.���β��������
ʵ������ⶨ�ù���������Һ������ķ�ˮ���軯�Ƶĺ�����
��֪���ٷ�ˮ���軯�Ƶ�����ŷű�Ϊ0.50mg/L��
��![]() ,
,![]() ��AgI�ʻ�ɫ��
��AgI�ʻ�ɫ��![]() ������
������![]() ��Ӧ��ʵ�����£�ȡ1L�������NaCN��ˮ��Ũ��Ϊ10.00mL������ƿ�У����μӼ���KI��Һ��ָʾ������
��Ӧ��ʵ�����£�ȡ1L�������NaCN��ˮ��Ũ��Ϊ10.00mL������ƿ�У����μӼ���KI��Һ��ָʾ������![]() mol/L�ı�
mol/L�ı�![]() ��Һ�ζ�������
��Һ�ζ�������![]() ��Һ�����Ϊ5.00mL��
��Һ�����Ϊ5.00mL��
(5)�ζ��յ��������__________________________________��
(6)������ķ�ˮ���軯�Ƶ�Ũ��Ϊ_________mg/L��������ķ�ˮ�Ƿ�ﵽ�ŷű���___________(����������������)��
��.(7)�����£���������Ҫ������ʽ����pHӰ�졣���õ绯ѧԭ�����ö��Ե缫��ⱥ��![]() ��ҺҲ�����Ʊ��������ơ���֪�������ŵ��������ҪΪ
��ҺҲ�����Ʊ��������ơ���֪�������ŵ��������ҪΪ![]() ����������Ӧ����ʽΪ_____________________��
����������Ӧ����ʽΪ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���װ�(CH3NH2)��һ��Ӧ�ù㷺��һԪ�������뷽��ʽΪ��CH3NH2+H2O![]() CH3NH3++OH�������£���20.0mL0.10mol/L�ļװ���Һ�еμ�VmL0.10mol/L��ϡ���ᣬ�����Һ��pH�������Ũ�ȵĹ�ϵ��ͼ��ʾ������˵���д�����ǣ� ��
CH3NH3++OH�������£���20.0mL0.10mol/L�ļװ���Һ�еμ�VmL0.10mol/L��ϡ���ᣬ�����Һ��pH�������Ũ�ȵĹ�ϵ��ͼ��ʾ������˵���д�����ǣ� ��
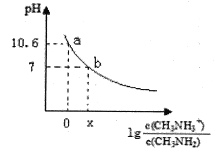
A. b���Ӧ������������V<20.00mL
B. �����£��װ��ĵ��볣��ΪKb����Kb=10��3.4
C. b����ܴ��ڹ�ϵ��c(Cl��)>c(CH3NH3+)>c(H+)>cOH��)
D. V=20.00mLʱ����Һ��ˮ�����c(H+)>10��7mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������100 mL 1.0 mol��LNa2CO3��Һ�����в�����ȷ����
A. ��ȡ10.6 g��ˮ̼���ƣ�����100 mL����ƿ�У���ˮ�ܽ⡢����
B. ��ȡ10.6 g��ˮ̼���ƣ�����100 mL����ˮ�����衢�ܽ�
C. ת��Na2CO3��Һʱ��δ�ò�����������ֱ�ӵ�������ƿ��
D. ���ݺ�����ƿ����������ת��ҡ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com