
【题目】可用于分离或提纯物质的方法有:过滤、蒸发结晶、蒸馏、萃取、分液、洗气。根据需求填下列装置的序号并填上操作名称:
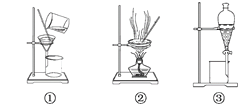
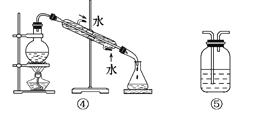
(1)分离Na2CO3溶液和CCl4,选_____,操作名称为________。
(2)用CCl4提取碘水中的碘,选______,操作名称为________。
(3)用氢氧化钠溶液吸收O2中混有的杂质Cl2,选_______,操作名称为________。
(4)除去澄清石灰水中悬浮的CaCO3颗粒选______,操作名称为__________。
(5)制取蒸馏水,选________,操作名称为________。
【答案】③ 分液 ③ 萃取(分液) ⑤ 洗气 ① 过滤 ④ 蒸馏
【解析】
(1)Na2CO3溶液和CCl4互不相溶;
(2)用CCl4提取碘水中的碘,水与四氯化碳互不相溶,分层,碘在四氯化碳中溶解度大;
(3)氯气可用氢氧化钠溶液除杂;
(4)CaCO3是不溶于水的物质;
(4)水的沸点不高;
(1)Na2CO3溶液和CCl4互不相溶,可用分液的方法分离;选③,操作名称为分液;
(2)用CCl4提取碘水中的碘,水与四氯化碳互不相溶,分层,碘在四氯化碳中溶解度大,可用萃取的方法分离;选③,操作名称为萃取(分液);
(3)氯气可用氢氧化钠溶液洗气,达到除杂的目的,选 ⑤,操作名称为洗气;
(4)根据CaCO3的溶解性,是不溶于水的物质,要和石灰水分离,可以采用过滤的方法;选①,操作名称为过滤;
(4)水的沸点不高,可选用蒸馏的方法制取;选④,操作名称为蒸馏。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是( )
A. 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B. 当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(O2)
C. 当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D. 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有32 g某气体,摩尔质量为16 g·mol-1,则:
①该气体为___________ mol。
②该气体所含分子数为___________ NA。
③该气体在标准状况下的体积为_________ L。
(2)实验室常用浓盐酸的质量分数为36.5%,密度为1.16g·mL-1,其物质的量浓度是_______
(3)若标况下X2的密度为1.43 g/L,X原子最外层有_____个电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种碳酸锰矿的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等。已知碳酸锰难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下:

(1)写出用稀硫酸溶解碳酸锰反应的离子方程式______________________________。
(2)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.3 |
沉淀完全的pH | 3.7 | 4.7 | 9.6 | 9.8 | 10.8 |
①流程中先加双氧水的目的是__________________________________________。
②加氨水调节溶液的pH等于6,则滤渣的成分是__________________,滤液中含有的阳离子有H+ 和___________________。
(3)在浸出液里锰元素只以Mn2+ 的形式存在,且滤渣中也无MnO2,请解释原因_________。
(4)阴离子膜法电解装置如右图所示,电解装置中箭头表示溶液中阴离子移动的方向,则A电极是______极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为__________________________。

(5)该工艺之所以采用阴离子交换膜,是为了防止Mn2+ 进入阳极区发生副反应生成MnO2造成资浪费,写出该副反应的电极反应式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法即李比希法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。
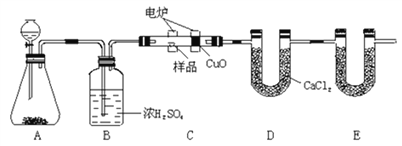
回答下列问题:
(1)A装置中分液漏斗盛放的物质是__________。
(2)写出E装置中所盛放物质的名称_________________,有学生认为在E后应再加一与E相同的装置,目的是_____________________。
(3)某有机化合物A经李比希法测得其中含碳为72.0%、含氢为6.67%,其余为氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的相对分子质量为150。
方法二:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3,如下图
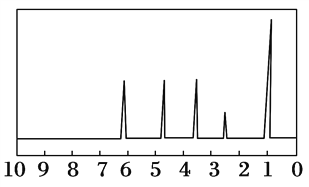
方法三:利用红外光谱仪测得A分子的红外光谱如下图所示。

请填空:
①A的分子式为________;结构简式为________
②A的芳香类同分异构体有多种,其中符合下列条件:
1)分子结构中只含一个官能团;2)分子结构中含有一个甲基;3)苯环上只有一个取代基。
则该类A的同分异构体共有____种,写出其中一种核磁共振氢谱有6个峰,且面积之比为1:1:1:2:2:3的同分异构体的结构简式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据元素周期表和周期律的相关知识,下列说法正确的是( )
A.短周期元素中,原子最外层只有一个或两个电子的元素一定是金属元素
B.I属于副族元素
C.H2S的稳定性比H2O的稳定性强
D.Na、Mg、Al与冷水反应速率逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的量的计算是中学化学的重要部分,请回答下列有关物质的量的计算问题。
(1)在标准状况下,67.2 L CO2是__________mol,质量为_______g,含有__________个CO2分子,其中含有__________mol氧原子。
(2)在标准状况下,1.7 g氨气所占的体积约为_________L,它与同条件下_____mol H2S含有相同的氢原子数。
(3)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为_______,R的相对原子质量为__________。
(4)实验室常用浓硫酸的质量分数为98%,密度为1.80 g·mL1,其物质的量浓度是_______。
(5)标准状况下,将V L A气体(摩尔质量为M g/mol)完全溶于0.1 L水(密度1 g/cm3)中,所得溶液的密度为d g/mL,则此溶液的物质的量浓度为_______mol/L。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. Na2CO3溶液显碱性,NaHCO3溶液显酸性
B. 可用加热方法除去NaHCO3固体中的Na2CO3杂质
C. 用Ba(OH)2溶液能鉴别碳酸钠和碳酸氢钠溶液
D. 等质量的Na2CO3、NaHCO3固体分别与足量盐酸反应,后者产生的CO2多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测得某溶液中含Cu2+ , K+ , SO42﹣ , Cl﹣四种离子且阳离子的个数比为:N(Cu2+):N(K+)=3:4,则SO42﹣与Cl﹣的物质的量之比可能是( )
A.3:2
B.1:3
C.1:8
D.2:5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com