
�����⻯�����������Ҫ�Ļ���ԭ�ϣ��ڹ�ũҵ�������й㷺��Ӧ�á��������е�NOx�����ѳ�����������������ŷš�
��1���ϳɰ�ԭ��������һ���Ʊ���ӦΪ��CO��H2O(g) CO2+H2
CO2+H2
��t��ʱ����1L�ܱ������г���0.2mol CO��0.3molˮ��������Ӧ����ƽ�����ϵ��c(H2)��0.12mol��L-1�����¶��´˷�Ӧ��ƽ�ⳣ��K��_________�������������
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1molCO������Ӧ���½���ƽ��ʱ��ˮ��������ת���ʦ�(H2O)��______________________��
��2��NH3��O2�ڲ�ϵ���������´�145��Ϳ�ʼ��Ӧ��
4NH3(g)��5O2(g) 4NO(g)��6H2O(g)��
4NO(g)��6H2O(g)��
��H��-905kJ��mol-1
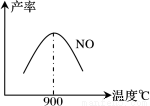
��ͬ�¶���NO������ͼ��ʾ���¶ȸ���900��ʱ��
NO�����½���ԭ��____________��
��3����֪��CH4(g)��2O2(g)��CO2(g)��2H2O(l)����H��-890.3kJ��mol-1
N2(g)��O2(g)��2NO(g)�� ��H����180kJ��mol-1
CH4���������������Ȼ�ѧ����ʽΪ______________________��
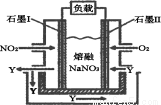
(4) ��NO2��O2������NaNO3��ɵ�ȼ�ϵ��װ������ͼ��ʾ��
��ʹ�ù�����ʯīI�缫��Ӧ����һ��������Y���йص缫
��Ӧ�ɱ�ʾΪ_________��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���ຣʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��Ԫ�����ڱ��У���3��4��5��6��������Ԫ�ص���Ŀ�ֱ��ǣ� ��
A. 8��18��32��32 B. 8��18��18��32 C. 8��18��18��18 D. 8��8��18��18
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��ɳ�и�����ѧ�ڵڶ����ܲ⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������������ԭ��Ϊ4NH3(g)+5O2(g)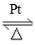 4NO(g)+6H2O(g)����Ũ��ˮ��ͨ������������Ȳ�˿���백ˮ��������Ӧ��˿���ֺ���״̬����Ӧֹͣ������˵����ȷ����
4NO(g)+6H2O(g)����Ũ��ˮ��ͨ������������Ȳ�˿���백ˮ��������Ӧ��˿���ֺ���״̬����Ӧֹͣ������˵����ȷ����
A��������Ӧ�ڽϸ��¶��²����Է�����
B���÷�Ӧ������Ӧ���С���淴Ӧ���
C���÷�Ӧ�У����ѻ�ѧ�����ܼ��ܴ����γɻ�ѧ�����ܼ���
D����NH3��O2�Ļ��������������Ӧ������ͨ������ˮ�У�ʣ������һ����O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ�����ѧ�ڵ�һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ������
������Ϊ12.64g KMnO4�������һ��ʱ����ռ���amolO2����Ӧ������Ĺ����м���������Ũ���ᣬ���ռ���bmolCl2����ʱMnԪ��ȫ����Mn2+����ʽ��������Һ�С�
��1������ɲ���ƽ���л�ѧ����ʽ��
K2MnO4+ HCl �� KCl+ MnCl2+ Cl2��+________��
�÷�Ӧ�еĻ�ԭ���� �����÷�Ӧ��ת��NA������ʱ��������������ʵ���Ϊ mol���������Ļ�ԭ�������ʵ���Ϊ mol��
��2�������Ը��������Һ�ζ�FeSO4��Һд���÷�Ӧ�����ӷ���ʽ ��
��3����KMnO4�����������O2 a molֵ���ʱ����Ӧ������Ĺ����м���������Ũ���Ტ���ȣ�����Cl2�����ʵ���b= mol��(��ʱMnԪ��ȫ����Mn2+����ʽ��������Һ��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ�����ѧ�ڵ�һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��NA��ʾ�����ӵ�������������˵������ȷ����
A��31g������������p��p���ۼ���ĿΪ1.5NA
B����״���£�2.24LD2���������ӵ���Ŀ��0.2NA
C�����³�ѹ��42g��ϩ�ͱ�ϩ�Ļ�����庬��ԭ����ĿΪ6 NA
D�������£���1L0.2mol/L��������Һͨ�백��������ҺPH=7ʱ����Һ��NH4+����ĿС��0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪�ֳ�����ʮһ�и�һ����ĩ����ѧ�������棩 ���ͣ�ѡ����
�йؼ������������ʾ����֪N2��g��+3H2��g���T2NH3��g����H=��92.4kJ•mol��1����x��ֵΪ�� ��
��ѧ�� | N��N | H��H | H��N |
����/kJ•mol��1 | x | 436 | 391 |
A��945.6 B��649 C��431 D��869
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪�ֳ�����ʮһ�и�һ����ĩ����ѧ�������棩 ���ͣ�ѡ����
���������缫������ϡH2SO4��Һ�У�Ȼ��ֱ�������ͨ��H2��O2�����ɲ�����������Ϊȼ�ϵ�أ�����������ȷ���ǣ� ��
��ͨ��H2�ĵ缫Ϊ�������������ĵ缫��Ӧ��O2+2H2O+4e���T4OH����
�������ĵ缫��Ӧ��O2+4e��+4H+�T2H2O���ܸ����ĵ缫��Ӧʽ��H2��2e��+2OH���T2H2O��
�ݸ����ĵ缫��Ӧʽ��H2��2e���T2H+���ŵ�ʱ��Һ�е����������ƶ���
A���٢ۢ� B���ڢܢ� C���ۢݢ� D���٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017����������߿���ѧ�����ѧ�Բ�ר����ԭ�ӽṹ�����ʣ������棩 ���ͣ������
��ͼ��ʾ����Ԫ������A��B��C��D��E���ֻ����ԲȦ���沿��ָ���ֻ����ﺬ��һ����ͬԪ�أ����ֻ����������ֶ�����Ԫ���γɣ�ÿ�ֻ������������Ԫ�أ�A����������Ҫ�ɷ֣�B��E������������������Ϊ18��B���ȶ������н�ǿ�������ԣ���ϡ��Һ��ҽ���Ϲ㷺ʹ�õ���������E�ķ��ӽṹģ��Ϊ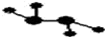 ��C����Ϊ���ά����Ҫ���ϣ�D����������Ԫ�ص�ԭ�Ӹ�����Ϊ3��4����������֮��Ϊ3��2������������Ϣ�ش��������⣺
��C����Ϊ���ά����Ҫ���ϣ�D����������Ԫ�ص�ԭ�Ӹ�����Ϊ3��4����������֮��Ϊ3��2������������Ϣ�ش��������⣺
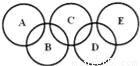
��1��BΪ��Ԫ���ᣬ��ˮ��Һ�������ԣ���B��ˮ��Һ�ĵ�һ�����뷽��ʽ�ɱ�ʾΪ ��
��2��D�Ļ�ѧʽ�� ��E����ʽΪ ��
��3��Һ̬B��Һ̬E��Ӧ������һ����̬���ʺ�һ�ֳ���Һ�壬1molB�μӷ�Ӧ�ų�����QkJ���䷴Ӧ���Ȼ�ѧ����ʽ ��
��4��NH3�����е�Nԭ����һ�Թ¶Ե��ӣ��ܷ�����Ӧ��NH3+HCl=NH4Cl��E��NH3�������ƣ�Ҳ����HCl������Ӧ����д��E���������ᷢ����Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ�����и߶���ĩͳ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
W��X��Y��Z��ԭ������������������ֶ�����Ԫ�أ���֪������Ԫ�صĵ��Ӳ���֮��Ϊ10�������Ƿֱ������������ĸ����壻����Ԫ�ص�ԭ���а뾶������Xԭ�ӡ�����˵����ȷ����
A. ����Ԫ����������Ԫ���ڵڶ�����
B. W��������Ԫ�ص�ԭ�Ӵ�������������Ϊ2��8��������Ϊ18
C. X��Y��Z������������Ӧ��ˮ��������֮���ܷ�Ӧ
D. ��ҵ�ϻ��X��Y���ʵķ�����Ҫ�ǵ�������ڵ��Ȼ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com