
(6分)分析下列反应:3S+6 KOH = 2K2S+K2SO3+3H2O,据此作答:
(1)用双线桥标出该反应中电子的转移方向和数目:3S +6 KOH = 2K2S+K2SO3+3H2O
(2)该反应的氧化产物是 。
(3)该反应的氧化剂与还原剂的质量比是 。
(4)当消耗0.3 mol S时,则转移的电子数是 。
(6分)(1) (2分);
(2分);
(2)K2SO3(1分);(3)2∶1(1分);(4)0.4 NA(2分);
【解析】
试题分析:(1)在3S +6 KOH = 2K2S+K2SO3+3H2O中,单质S由反应前的0价,变为反应后K2S的-2价,化合价降低,得到电子,作氧化剂;由反应前的0价,变为反应后K2SO3的+4价,化合价升高,失去电子;作还原剂。用双线桥法表示为 .在该反应中S作还原剂,失去电子被氧化变为K2SO3,所以K2SO3是氧化产物;(3)S作氧化剂,得到电子被还原变为还原产物K2S。在反应中氧化剂与还原剂的物质的量的比为2:1;由于是同一种物质,所以物质的量的比为质量比,因此该反应的氧化剂与还原剂的质量比是2:1;(4)根据方程式可知,每有3mol的S发生反应,会转移电子4mol,所以当消耗0.3 mol S时,则转移的物质的量是0.4mol,由于阿伏伽德罗常数是NA,所以转移的电子数是0.4 NA。
.在该反应中S作还原剂,失去电子被氧化变为K2SO3,所以K2SO3是氧化产物;(3)S作氧化剂,得到电子被还原变为还原产物K2S。在反应中氧化剂与还原剂的物质的量的比为2:1;由于是同一种物质,所以物质的量的比为质量比,因此该反应的氧化剂与还原剂的质量比是2:1;(4)根据方程式可知,每有3mol的S发生反应,会转移电子4mol,所以当消耗0.3 mol S时,则转移的物质的量是0.4mol,由于阿伏伽德罗常数是NA,所以转移的电子数是0.4 NA。
考点:考查氧化还原反应方程式的表示、物质的作用、转移的电子数的计算的知识。
考点分析: 考点1:氧化还原反应 试题属性

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源:2014-2015学年湖南省长望浏宁四县高三一模考试化学试卷(解析版) 题型:填空题
(14分)磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中高温(~1550℃)下通过下面三个反应共熔得到。
①4Ca3(PO4)2(s)+10C(s)=12CaO(s)+2P4(s)+10CO2(g) ΔH1=+Q1kJ·mol-1
②CaO(s)+SiO2(s)=CaSiO3(s) ΔH2=-Q2 kJ·mol-1
③CO2 (g)+C(s)=2CO(g) ΔH3=+Q3kJ·mol-1
已知:CaSiO3的熔点(1546℃)比SiO2低。
a、写出由磷酸钙矿制取白磷总的反应方程式_____________________________。
b、上述反应中SiO2起何作用?______________________________________。
(2)白磷在热的浓氢氧化钾溶液中岐化得到一种次磷酸盐(KH2PO2)和一种气体 (写化学式)。
(3)磷的重要化合物NaH2PO4可通过H3PO4与NaOH溶液反应获得。工业上为了使反应的主要产物是NaH2PO4,通常将pH控制在 之间 (已知磷酸的各级电离常数为:K1 = 7.1×103 K2 = 6.3×108 K3 =4.2×1013 lg7.1≈0.9 lg6.3≈0.8 lg≈0.6) 。Na2HPO4 溶液显碱性,若向溶液中加入足量的CaCl2 溶液,溶液则显酸性,其原因是 (用离子方程式表示)。
(4)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示:
11P 4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
60molCuSO4能氧化白磷的物质的量是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市高三下学期开学联考化学试卷(解析版) 题型:选择题
下列四种基本类型的反应中,一定是氧化还原反应的是
A.分解反应 B.置换反应 C.复分解反应 D.化合反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将甲针筒内的物质压到乙针筒内,进行实验,对乙针筒里的现象所作的判断不正确的是
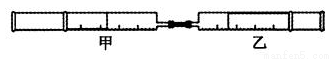
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 乙针筒里的现象 |
A | HCl | AgNO3溶液 | 产生白色沉淀 |
B | NH3 | FeCl3溶液 | 出现红褐色沉淀 |
C | CO2 | BaCl2 | 产生白色沉淀 |
D | Cl2 | 紫色石蕊溶液 | 先变红后褪色 |
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:推断题
(9分)有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。请根据以上信息回答下列问题:
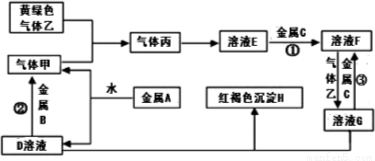
(1)写出下列物质的化学式:乙 、H ;
(2)写出反应②的离子方程式: ;
(3)写出金属A与水反应的离子方程式 ;
(4)F与D溶液反应后的产物在空气中转化为H的化学方程式 ;现象为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
某废液中含有Ba2+、Ag+和Cu2+,用 ①Na2CO3溶液、②NaOH溶液、③盐酸三种试剂将它们逐一沉淀并加以分离,加入试剂的正确顺序是
A.②-①-③ B.①-②-③ C.③-②-① D.③-①-②
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
下列有关物质的性质或用途的说法中,正确的是
① 氯气具有漂白性,可以使有色布条褪色
② 明矾在水中能生成Al(OH)3胶体,可用作净水剂
③ Si可用于制造光导纤维
④ SiO2、Na2CO3和CaCO3可用于制玻璃
⑤ 水玻璃可用于生产防火材料
⑥ 铁红常用作红色油漆和涂料
A.①②③⑤ B.②④⑤⑥ C.③④⑤⑥ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:选择题
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g) N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
A | B | C | D |
|
|
|
|
升高温度,平衡常数减小 | 0~3s内,反应速率为: v(NO2)=0.2 mol·L-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.有单质生成的分解反应一定是氧化还原反应
B.某元素从化合态变为游离态时,该元素一定被还原
C.氧化剂被氧化,还原剂被还原
D.没有氧元素参加的反应一定不是氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com