
| A、硼电负性和硅相近 |
| B、BCl3、PCl5、H2O三种分子的中心原子的最外层电子均不满足8e-稳定结构 |
| C、原子和其它原子形成共价键时,其共价键数一定等于原子的价电子数 |
| D、组成和结构相似的物质随相对分子质量的增大,熔沸点升高,所以NO的沸点应该介于N2和O2之间 |


科目:高中化学 来源: 题型:
| A、聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 |
| B、棉花、木材和羊毛的主要成分都是纤维素 |
| C、pH在5.6-7.0之间的降水通常称为酸雨 |
| D、汽油、植物油、甘油都有特殊的香味,都是酯类 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | … | 29 |
| C2H6 | C2H6O | C2H4O2 | C3H8 | C3H8O | C3H6O2 | C4H10 | … | X |
| A、X的分子式为C11H24O |
| B、X可能与金属钠反应生成氢气 |
| C、X可能与碳酸钠反应放出CO2气体 |
| D、X可能与第30项发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、合成纤维和光导纤维都是新型无机非金属材料 |
| B、乙醛、氯乙烯和乙二醇均可作为合成聚合物的单体 |
| C、淀粉、纤维素的化学式都可表示为(C6H10O5)n,二者互为同分异构体 |
| D、乙醛、乙酸和葡萄糖都能与新制的Cu(OH)2反应,且反应类型均为氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、绿色化学的核心是应用化学原理对环境污染进行治理 |
| B、氯气和氢氧化钠溶液和石灰乳得到的含氯化合物都具有漂白性 |
| C、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
| D、对“地沟油”蒸馏可以获得汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 请回答下列问题.
请回答下列问题.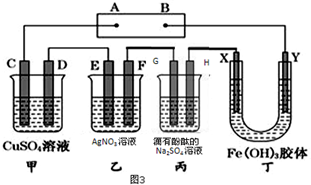
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致 |
| B、铁在潮湿的空气中放置,易发生化学腐蚀而生锈 |
| C、绿色化学的核心是从源头上消除工业生产对环境的污染 |
| D、用CO2合成聚碳酸酯可降解塑料,可实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
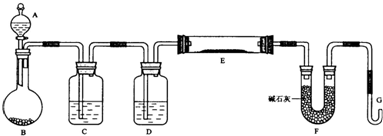
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com