

 ;这样制取的溴苯可以用AD洗涤除Br2.
;这样制取的溴苯可以用AD洗涤除Br2.

 FeBr3+
FeBr3+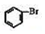 +HBr;该小组将A装置中浓硫酸替换成稀硫酸时实验失败,试从反应机理推测可能的原因是有水情况下,无法生成Br+.
+HBr;该小组将A装置中浓硫酸替换成稀硫酸时实验失败,试从反应机理推测可能的原因是有水情况下,无法生成Br+. 分析 c装置发生反应:MnO2+2NaBr+2H2SO4$\frac{\underline{\;加热\;}}{\;}$Br2↑+MnSO4+Na2SO4+2H2O,制备溴单质,为防止溴蒸汽冷凝,在A中对广口瓶进行热水浴,溴蒸汽在D中与苯发生反应: ,最后在硝酸银中吸收未反应溴蒸汽和溴化氢,防止污染空气,据此分析作答;
,最后在硝酸银中吸收未反应溴蒸汽和溴化氢,防止污染空气,据此分析作答;
(1)根据常见仪器的结构和功能确定仪器X的名称;实验室用苯和溴在催化剂的作用下反应制备溴苯;溴苯难溶于水,而Br2能溶于NaOH溶液,且其氧化性强,能氧化还原性较强的Na2SO3溶液;
(2)①溴蒸汽由C制备,由d到a进入热水浴防止冷凝,由c到e进入D中反应,在B中吸收尾气,则顺序为d、a、b、e、f、c;
③混合液后,D中液体沸腾,可根据该反应是放热反应分析;
(3)为防止Br2蒸气冷凝,A中对广口瓶进行热水浴;
(4)溴蒸汽可与硝酸银反应生成沉淀,B中有淡黄色沉淀生成,不能确定苯与液溴发生了取代反应;
Ⅱ.①第三步反应为溴苯的生成,化学反应为: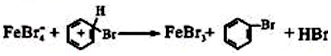 ;
;
解答 解:(1)仪器X为球形冷凝管;实验室用苯和溴在催化剂的作用下反应制备溴苯,化学方程式为: ;
;
A.Br2氧化性强,能氧化Na2SO3溶液,生成易溶于水的盐,有利于分液分离,故A正确;
B.Br2易溶于溴苯,而微溶于难水,无法通过分液进行分离,故B错误;
C.乙醇与水混溶,且是良好的有机溶剂,无法分层,不可分液分离,故C错误;
D.Br2能溶于NaOH溶液,生成易溶于水的盐,有利于分液分离,故D正确;
答案为AD;
故答案为:球形冷凝管; ;AD;
;AD;
(2)①溴蒸汽由C制备,由d到a进入热水浴防止冷凝,由c到e进入D中反应,在B中吸收尾气,则顺序为d、a、b、e、f、c;
故答案为:a;b;e;f;
③C中加入固体药品,C处滴加浓硫酸,再打开D处开关K,点燃C处酒精灯,制得溴蒸汽反应;该反应是放热反应,插入铁丝于混合液中,一段时间后,D中液体沸腾;
故答案为:该反应是放热反应;
(3)为防止Br2蒸气冷凝,A中对广口瓶进行热水浴;
故答案为:防止溴单质蒸气冷凝;
(4)Br2有挥发性,溴蒸汽可与硝酸银反应生成淡黄色沉淀;
故答案为:否;D中会挥发出少量的Br2,Br2也可以和硝酸银产生淡黄色沉淀;
Ⅱ.第三步反应为溴苯的生成,化学反应为: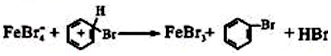 ;将A装置中浓硫酸替换成稀硫酸时实验失败,有水情况下,无法生成Br+;
;将A装置中浓硫酸替换成稀硫酸时实验失败,有水情况下,无法生成Br+;
故答案为: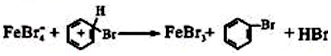 ;有水情况下,无法生成Br+.
;有水情况下,无法生成Br+.
点评 本题主要考查了溴苯的制备,学生知识综合应用、根据实验目的及物质的性质进行排列顺、实验基本操作能力及实验方案设计能力,综合性较强,注意把握物质性质以及对题目信息的获取于使用,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 残余固体全部是铜 | |
| B. | 残余固体可能为铁和铜的混合物 | |
| C. | 最后得到的溶液可能含有Fe3+ | |
| D. | 残余固体是铁,溶液中一定不含Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某工厂用电解法处理含有SO2的尾气,其装置如图所示(电极材料均为惰性电极),下列说法不正确的是( )
某工厂用电解法处理含有SO2的尾气,其装置如图所示(电极材料均为惰性电极),下列说法不正确的是( )| A. | 电极a连接的是电源的正极 | |
| B. | 若电路中转移0.03mol e-,则离子交换膜左侧溶液中增加0.03mol离子 | |
| C. | 图中的离子交换膜是阳离子交换膜 | |
| D. | 阴极的电极反应式为2HSO3-+2e-+2H+═S2O42-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ③④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的稀硝酸与碳酸钠 | B. | 过量的浓盐酸与二氧化锰 | ||
| C. | 过量的铜与浓硫酸 | D. | 过量的锌与18mol/L硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数为6 | B. | 质子数为6 | ||
| C. | 电子数为14 | D. | C的相对原子质量为14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3p2表示3p上有两个杂化轨道 | |
| B. | 处于最低能量的原子叫做较低能量的激发态原子 | |
| C. | 原子中,2p、3p、4p 具有相同的轨道数 | |
| D. | 原子中,1s、2s、3s电子的能量逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||
| Y | Z | W |
| A. | 原子半径:Y>Z>X | |
| B. | 化合物YX2和ZX2含有的化学键类型相同 | |
| C. | Z元素的氧化物对应水化物的酸性一定比W的弱 | |
| D. | Y、W元素能形成化学式为YW4的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com