
常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是
A.0.1mol·L-1NaHCO3溶液中的粒子浓度:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)>c(OH-)>c(H+)
B.将标况下2.24L的CO2通入150mL 1mol·L-1NaOH溶液中充分反应后的溶液:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3)
C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合溶液的pH等于7,则反应后的混合液:2c(R2-)+c(HR-)>c(Na+)
D.0.2 mol·L-1的某一元酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:c(OH-)+2c(A-)=c(H+)+2c(HA)
B
【解析】
试题分析:A、碳酸氢钠溶液中存在碳酸氢根离子的电离和水解,水解程度大于其电离程度,所以溶液层碱性,则不水解的离子钠离子的浓度最大,其次为碳酸氢根离子,然后是水解产生的氢氧根离子,所以粒子的浓度关系是c(Na+)>c(HCO3-)> c(OH-)>c(H2CO3)> c(H+) >c(CO32-),错误;B、标准状况下2.24L二氧化碳的物质的量是0.1mol,与0.15molNaOH反应,则Na元素的物质的量浓度与C元素的物质的量浓度之比是0.15:0.1=3:2,根据物料守恒,则2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3),正确;C、pH=3的二元弱酸中氢离子浓度与氢氧化钠溶液混合后溶液pH=7,为中性,则c(OH-)=c(H+),根据电荷守恒,则c(OH-)+2c(R2-)+c(HR-)=c(H+)+ c(Na+),所以2c(R2-)+c(HR-)=c(Na+),错误;D、0.2 mol·L-1的某一元酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后,得到的溶液为等浓度的HA和NaA的混合液,溶液pH>7,说明混合液为碱性,A-的水解程度大于HA的电离程度,根据物料守恒,则2c(Na+)= c(A-)+ c(HA),根据电荷守恒,有c(OH-)+c(A-)=c(H+)+c(Na+),两式联立,消去c(Na+),可得2c(OH-)+c(A-)=2c(H+)+c(HA),错误,答案选B。
考点:考查电解质溶液中离子浓度的比较,守恒规律的应用


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年河北省高三第五次调研考试化学试卷(解析版) 题型:简答题
(14分)甲醇是一种重要的化工原料,在生产中有着重要的应用。工业上用甲烷氧化法合成甲醇的反应有:
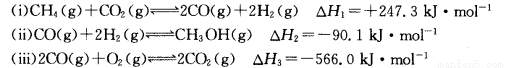
(1)用CH4和02直接制备甲醇蒸气的热化学方程式为 。
(2)某温度下,向4 L恒容密闭容器中通人6 mol C02和6mol CH4,发生反应(i),平衡体系中各组分的体积分数均为 ,则此温度下该反应的平衡常数K= ,CH4的转化率为 。
,则此温度下该反应的平衡常数K= ,CH4的转化率为 。
(3)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为:
 ,科研人员对该反应进行了研究,部分研究结果如下:
,科研人员对该反应进行了研究,部分研究结果如下:


①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是 (填“3.5× 106 Pa” “4.O×106 Pa”或“5.0× 106 Pa”)。
②实际工业生产中采用的温度是80℃,其理由是 。
(4)直接甲醇燃料电池(简称DMFC)由于其结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:

①通入a气体的电极是电池的 (填“正”或“负”)极,其电极反应式为 .
②常温下,用此电池以惰性电极电解O.5 L饱和食盐水(足量),若两极共生成气体1.12 L(已折算为标准状况下的体积),则电解后溶液的pH为 (忽略溶液的体积变化)。
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列常见金属的冶炼原理中不合理的是
金属 | 冶炼原理 | |
A | Fe | Fe2O3+3CO= |
B | Hg | 2HgO |
C | Mg | 2MgO(熔融)= |
D | Na | 2NaCl(熔融)= |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省濉溪县高三第二次月考化学试卷(解析版) 题型:选择题
向四支盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如下图所示:
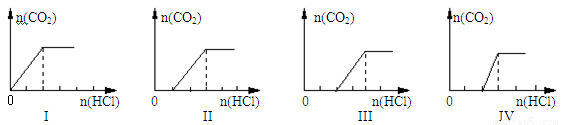
则下列分析都正确的组合是
选项 | 溶质的成分 | 对应图象 | 溶液中离子浓度关系 |
A | NaHCO3 | I | c(Na+) = c(HCO3-) |
B | NaOH、Na2CO3 | Ⅳ | c(OH-)>c(CO32-) |
C | Na2CO3 | Ⅲ | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
D | NaHCO3、Na2CO3 | Ⅱ | c(CO32-)>c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省濉溪县高三第二次月考化学试卷(解析版) 题型:选择题
下列有关说法合理的是
A.根据分散系是否有丁达尔现象,将分散系分为胶体、浊液和溶液
B.用盐酸可以清洗长期存放过FeCl3溶液的试剂瓶
C.二氧化硅广泛用于制作计算机芯片和光导纤维
D.电解精炼铜时,阳极泥中含有Fe、Ag、Au等金属
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省安庆五校联盟高三下学期3月联考理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列说法中正确的是
A.100mL 1mol·L-1AlCl3溶液中含的阳离子数等于0.1NA
B.标准状况下,22.4L CCl4中含有的CCl4分子数为NA
C.将2mL 0.5mol·L-lNa2SiO3溶液滴入稀盐酸中制得H2SiO3胶体,所含胶粒数为0.001NA
D.一定条件下,2.3gNa完全与O2反应生成3.6g产物时失去的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三下学期初考理综化学试卷(解析版) 题型:选择题
某恒温密闭容器中,可逆反应A(s) B+C(g) ΔH= +Q kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
B+C(g) ΔH= +Q kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
A.产物B的状态只能为固态或液态
B.平衡时,v(A)消耗﹕n(C)消耗=1﹕1
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q kJ
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期中化学试卷(解析版) 题型:选择题
化学方程式可简明地体现元素及其化合物的性质。
已知:

下列说法不正确是:
A.酸性(水溶液):HSCN〉H2CO3〉HCN
B.还原性(碱性溶液):Fe(OH)2〉I—〉KIO3
C.热稳定性:NaCl〉NaClO4〉NaClO
D.氧化性(酸性溶液):I2〉FeCl3〉Co(OH)3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北大冶一中等六校高三元月调考理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列叙述正确的是
A.6.8g熔融的KHSO4中含有0.05NA个阴离子
B.1.0L 1mol/L的NaOH水溶液中含有的氧原子数目为NA
C.25 ℃时,pH=13的氢氧化钡溶液中含有0.1NA个氢氧根离子
D.5.6g铁与一定量稀硝酸完全反应,电子转移数目一定为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com