
| A、原子电子层数的多少 |
| B、最外层电子数的多少 |
| C、最高价氧化物的水化物的碱性强弱 |
| D、等物质的量的金属置换氢气的多少 |


科目:高中化学 来源: 题型:
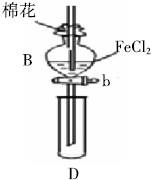 某探究学习小组用如图所示装置进行SO2、Fe3+和Cl2氧化性强弱比较实验,实验过程如下:
某探究学习小组用如图所示装置进行SO2、Fe3+和Cl2氧化性强弱比较实验,实验过程如下:| 过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 | |
| 甲 | 既有Fe3+又有Fe2+ | 有SO42- |
| 乙 | 有Fe3+ 无Fe2+ | 有SO42- |
| 丙 | 有Fe2+ 无Fe3+ | 有Fe2+ |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、35.5a=(w2-w1 )V2 | ||
B、n(Al)>
| ||
C、n(Na)+3n(Al)=
| ||
D、aV2=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有些金属晶体比原子晶体熔沸点高 |
| B、晶体只要有阴离子就一定有阳离子 |
| C、原子晶体中一定有非极性共价键 |
| D、分子晶体中不一定有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4和CH3CH3 |
| B、CH3-CH2-Cl和CH2Cl-CH2Cl |
| C、CH2=CHCH2CH3和CH3CH=CHCH3 |
D、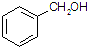 和 和 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高温 高压 |
| B、低温 低压 |
| C、高温 低压 |
| D、高压 低温 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com