
【题目】对于反应3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O,以下叙述正确的是( )
5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的氯原子和被还原的氯原子的物质的量之比为5:1
C.Cl2既做氧化剂又做还原剂
D.氧化剂得电子数与还原剂失电子数之比为5:1
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 放热的反应在常温下一定很易发生
B. 吸热反应在一定条件下也能发生
C. 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D. 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应在较低温度下能自发进行,较高温度下不能自发进行。下列有关该反应的说法正确的是
A. △H>0,△S>0 B. △H<0,△S<0 C. △H<0,△S>0 D. △H>0,△S<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.2mol水的摩尔质量是36g?mol﹣1
B.一个钠原子的实际质量约等于 ![]() ?g
?g
C.1.5mol O2的体积约为33.6L
D.将 100mL水加入到 100mL 1mol/L的NaOH溶液中,所得溶液为0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质递变的情况中,错误的是( )
A. Li、Be、B原子最外层电子数依次增多
B. P、S、Cl元素最高化合价依次升高
C. N、O、F原子半径依次增大
D. P、S、Cl元素的最低化合价依次为﹣3、﹣2、﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)在加热的条件下,用MnO2与100mL物质的量浓度为12mol/L的浓盐酸反应,制得氯气2.24L(标准状况)反应方程式为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,请用双线桥法标出该反应的电子转移的方向和数目 .
MnCl2+Cl2↑+2H2O,请用双线桥法标出该反应的电子转移的方向和数目 .
(2)上述反应的还原剂是;被还原的元素是 .
(3)需要消耗MnO2多少克?若反应后溶液的体积不变,则反应后溶液中Cl﹣物质的量浓度是多少?(请在答卷上写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体.相应的实验过程如图: 
(1)写出实验过程中所用试剂(写化学式):
试剂①;试剂③ .
(2)判断试剂①已过量的方法是: .
(3)用离子方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯.
操作①的实验结果:淀粉(填“能”或“不能”)透过半透膜;SO42﹣(填“能”或“不能”)透过半透膜.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )

A.a为负极,b为正极
B.d为阳极,c为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO![]() 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
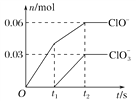
A. 反应中转移电子的物质的量是0.21 mol
B. ClO![]() 的生成可能是由于温度升高引起的
的生成可能是由于温度升高引起的
C. 标准状况下有3.36 L氯气参加反应
D. 苛性钾溶液中KOH的物质的量为0.2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com