
分析 (1)原电池中失电子的电极是负极,负极失电子发生氧化反应,正极上氧化剂得电子发生还原反应;
(2)根据溶液中氢氧根离子浓度是否变化判断;
(3)燃料电池中甲烷的利用率较高.
解答 解:(1)甲烷失电子发生氧化反应,所以通入燃料的电极为负极,通入氧化剂的电极为正极,正极上电极反应式为:O2+2H2O+4e-=4OH-,负极上甲烷失电子生成碳酸根离子和水,则负极的电极方程式为:CH4+10OH--8e-═CO+7H2O;
故答案为:正极;CH4+10OH--8e-═CO+7H2O;
(2)已知CH4+2O2+2KOH═K2CO3+3H2O,电池工作一段时间后,因为消耗氢氧化钾所以溶液的碱性减小,
故答案为:减小;
(3)甲烷燃烧时要放出热量、光能,所以燃料电池中甲烷的利用率比甲烷燃烧的能量利用率高,故答案为:大于.
点评 本题考查了燃料电池,明确原电池正负极上发生的反应是解本题关键,注意溶液的酸碱性对电极反应的影响,题目难度中等,侧重于考查学生的分析能力.


科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③⑤ | C. | ②④⑤ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
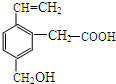 某有机物的结构为如图所示,这种有机物可能具有的性质是( )
某有机物的结构为如图所示,这种有机物可能具有的性质是( )| A. | ①②④ | B. | ①②③④⑤ | C. | ①③④⑤⑥ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
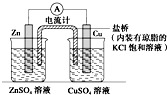
| A. | 该装置中电子由Zn极流向Cu极,CuSO4溶液中的SO41-通过盐桥移向Zn极 | |
| B. | 若装置中的两烧杯中均为CuSO4溶液,则电流计的指针偏转幅度变小,且很快减弱 | |
| C. | 将装置中烧杯内的溶液对换,电流计的指针也能发生偏转 | |
| D. | 将盐桥改为铜导线连接两种溶液,电流方向为由Cu极到Zn极 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该溶液的体积变为0.8L | B. | 该溶液的物质的量浓度为0.5mol/L | ||
| C. | 该溶液的物质的量为0.5mol | D. | 该溶液的物质的量浓度为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com