
【题目】根据反应中质子(H+)的转移,可以重新定义酸和碱:酸=质子+(共轭)碱。因此酸碱之间存在彼此的共轭关系:HA+BA-+BH+。关于反应:HC2O4-+H3O+![]() H2C2O4+H2O、HC2O4-+OH-
H2C2O4+H2O、HC2O4-+OH-![]() C2O42-+H2O,下列判断正确的是
C2O42-+H2O,下列判断正确的是
A. HC2O4-的共轭碱为H2C2O4
B. HC2O4-的共轭酸为C2O42-
C. HC2O4-既有酸性又有碱性
D.H3O+是水的共轭碱,H2O是OH-的共轭酸
【答案】C
【解析】
根据定义,酸=质子+(共轭)碱,反应HC2O4-+H3O+H2C2O4+H2O,可认为H3O+中的质子给了HC2O4-得到了H2C2O4和H2O,则H3O+是酸,其共轭碱是H2O;H2C2O4是酸,其共轭碱是HC2O4-;反应HC2O4-+OH-![]() C2O42-+H2O,可认为HC2O4-中的质子转移给了H2O,则HC2O4-是酸,其共轭碱是C2O42-;H2O是酸,其共轭碱是OH-。
C2O42-+H2O,可认为HC2O4-中的质子转移给了H2O,则HC2O4-是酸,其共轭碱是C2O42-;H2O是酸,其共轭碱是OH-。
A.根据分析,HC2O4-的共轭碱是C2O42-,A错误;
B.根据分析,HC2O4-的共轭酸为H2C2O4,B错误;
C.根据分析,HC2O4-是H2C2O4的共轭碱,是C2O42-的共轭酸,说明其既是酸又是碱,既有酸性又有碱性,C正确;
D.根据定义可推知,H3O+是水的共轭酸,D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W、Z同主族,Y的族序数等于其周期数,X、Y、Z的最外层电子数之和等于10,W、Z形成的一种化合物能使品红溶液褪色。下列说法正确的是( )
A.原子半径:W>X>Y>Z
B.W、X、Y三种元素组成的化合物的水溶液呈中性
C.常温下,Y易溶于Z的最高价氧化物对应的水化物的浓溶液
D.W、X、Z三种元素组成的某种化合物与盐酸反应时,可能有单质Z析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新研究表明,咖啡中含有的咖啡酸能使人心脑血管更年轻。咖啡酸的球棍模型如图所示,下列有关咖啡酸的叙述不正确的是( )

A.咖啡酸的分子式为C9H8O4
B.咖啡酸中的含氧官能团只有羧基、酚羟基
C.咖啡酸可以发生氧化反应、消去反应、酯化反应、加聚反应
D.![]() 是咖啡酸的一种同分异构体,1mol该物质最多可消耗3molNaOH
是咖啡酸的一种同分异构体,1mol该物质最多可消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铬(CrN)薄膜具有韧性高、耐磨性好、涂层结合强度高、更好的抗高温氧化性和抗腐蚀性以及内应力低等优点,在汽车工业、航空航天等领域取得了很好的应用效果。某化学兴趣小组利用下列装置进行氮化铬的制备(部分夹持装置已略),回答下列问题:
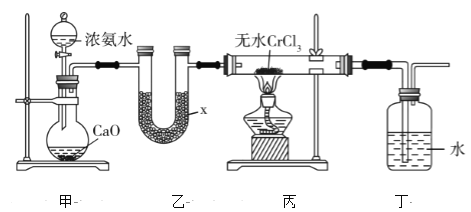
(1)仪器x的名称为________,x中盛有的试剂为干燥剂,该干燥剂可以是________(填字母)。
a.浓硫酸 b.碱石灰 c.CaO d.无水CaCl2
(2)装置甲中CaO可用NaOH固体代替,其原因是_______________________________________________。
(3)若装置丙玻璃管中产生大量白烟,则发生反应的化学方程式为__________________________________。
(4)装置丁洗气瓶中水的作用是________________________________________。该装置是否合适?合适则写出合适的理由,不合适则说明改进措施:_____________________________________________________
(5)实验前,在装置丙中加入15.850g CrCl3,实验结束后,取出装置丙中的固体加热至质量不再减少,称量剩余固体质量为7.525g,则制备的产品纯度为______%(保留小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.  与
与![]() 含有相同的官能团,互为同系物
含有相同的官能团,互为同系物
B. 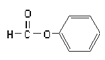 属于醛类,官能团为-CHO
属于醛类,官能团为-CHO
C. ![]() 的名称为:2-乙基-1-丁烯
的名称为:2-乙基-1-丁烯
D. ![]() 的名称为:2-甲基-1,3-二丁烯
的名称为:2-甲基-1,3-二丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化物NaBH4(B元素的化合价为+3价)燃料电池(DBFC), 由于具有效率高、产物清洁无污染和燃料易于储存和运输等优点,被认为是一种很有发展潜力的燃料电池。其工作原理如下图所示,下列说法正确的是
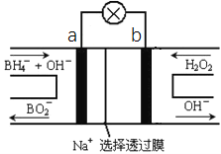
A. 电池的负极反应为BH4-+2H2O-8e-=BO2-+8H+
B. 放电时,每转移2mol电子,理论上需要消耗9.5gNaBH4
C. 电池放电时Na+从b极区移向a极区
D. 电极a采用MnO2,MnO2既作电极材料又有催化作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。当向其中加入少量酸或碱时,溶液的酸碱性变化不大。回答下列问题:
(1)将该溶液两等分,向其中加入少量盐酸时,发生反应的离子方程式为______;另一份加入少量KOH溶液时,发生反应的离子方程式为______。
(2)现将0.04molL-1HA溶液和0.02molL-1NaOH溶液等体积混合,得到缓冲溶液。
①若HA为HCN,该缓冲溶液显碱性,则溶液中c(Na+)______c(CN-)。(填“<”“=”或“>”);
②若HA为CH3COOH,该缓冲溶液显酸性。则溶液中所有的离子按浓度由大到小排列的顺序是______。
(3)缓冲溶液一般是由浓度较大的弱酸及其共轭碱所组成,其pH值的近似计算公式为:pH=pK酸+lg[c共轭碱/c酸]。人体血液中的H2CO3-HCO3-平衡起到缓冲作用。实测某人血液的pH=7.2,c(![]() )=2.3×10-2mol/L,且已知血液中的H2CO3的pKa1=6.2。则此人血液中的c(H2CO3)=______mol/L。
)=2.3×10-2mol/L,且已知血液中的H2CO3的pKa1=6.2。则此人血液中的c(H2CO3)=______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素D又称麻黄碱是一种天然的生物碱。天然麻黄素D的结构如图所示:
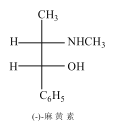
已知D的合成路线如下:
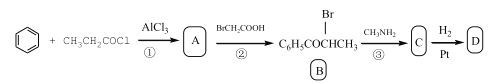
回答下列问题:
(1)写出反应①的化学方程式:______。指出其反应类型______。
(2)指出B中的官能团的名称______、D分子中有______个手性碳原子。
(3)出C→D的化学方程式:______。
(4)同时符合下列条件的C的同分异构体(不计立体异构)的数目共______种。
①属于对位二取代苯
②含有酰胺基(-CONH2)
(5)已知:R——NO2![]() R——NH2、氨基有碱性且易被氧化。设计一条由
R——NH2、氨基有碱性且易被氧化。设计一条由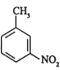 和乙醇为原料,制备
和乙醇为原料,制备 的合成路线______(无机试剂任选)。
的合成路线______(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的回收利用是环保领域研究热点。
(1)在太阳能的作用下,以CO2为原料制炭黑的流程如图所示。总反应的化学方程式为__;
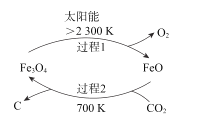
(2)有一种用CO2生产甲醇燃料的方法:CO2+3H2![]() CH3OH+H2O。
CH3OH+H2O。
已知298K和101kPa条件下:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(l) ΔH=-akJ/mol;
CH3OH(g)+H2O(l) ΔH=-akJ/mol;
2H2(g)+O2(g)=2H2O(l) ΔH=-bkJ/mol;
CH3OH(g)=CH3OH(l) ΔH=-ckJ/mol;
则CH3OH(l)的标准燃烧热ΔH=__;
(3)在催化剂M的作用下,CO2经过催化氢化合成低碳烯烃等。
CO2和H2同时发生下列两个反应:
①2CO2(g)+6H2(g) ![]() CH2=CH2(g)+4H2O(g) ΔH<0
CH2=CH2(g)+4H2O(g) ΔH<0
②2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH<0
CH3OCH3(g)+3H2O(g) ΔH<0
如图是乙烯在相同时间内,不同温度下的产率,当温度高于460℃时乙烯产率降低的原因不可能是__。
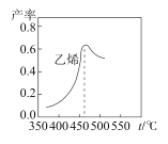
A.催化剂M的活性降低
B.①反应的平衡常数变大
C.生成甲醚的量增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com