
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O=2H++C1-+C1O- | |
| B. | 硫酸铝溶液中加入足量氨水:Al3++4OH-=AlO2-+2H2O | |
| C. | FeS04溶液与稀硝酸反应:3Fe2++NO3-+4H+=3Fe3++NO+2H2O | |
| D. | 稀硫酸中加入铁粉:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界的硫元素主要以硫单质、硫化物和硫酸盐等形式存在 | |
| B. | 浓硫酸可作干燥剂,但不能干燥二氧化硫、氯气等气体 | |
| C. | 二氧化硫能使溴水褪色,说明其具有漂白性 | |
| D. | 浓硫酸中存在的主要是硫酸分子,常温下就能和铜片剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤⑦ | B. | ⑥ | C. | ⑥⑦ | D. | ⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CO2中混有的少量SO2,可将气体通过酸性高锰酸钾溶液 | |
| B. | 除去SiO2中混有的少量Al2O3,可以用NaOH溶液洗涤 | |
| C. | 除去Fe粉中的少量Mg粉,可以将该粉末用稀硝酸洗涤,然后过滤 | |
| D. | 除去NO2气体中混有的少量NO气体,可以向该气体中充入过量空气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应进行60s时,X、Y、Z的浓度相等 | |
| B. | 反应进行80s时,逆反应速率大于正反应速率 | |
| C. | 以X浓度变化表示的反应速率为0.06mol/(L•min) | |
| D. | 反应进行80s时,Y物质的量浓度为0.03mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
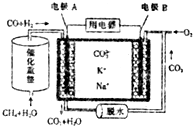
| A. | 电流方向:由B极经用电器流向A极 | |
| B. | 电极B上发生的电极反应为2CO2+O2+4e-═CO22- | |
| C. | 电池工作时,K+、Na+向电极B移动 | |
| D. | 若消耗电极B上的O233.6L(标准状况),则至少需要1moL CH4参加反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.0g草酸中共用电子对数目为0.9NA | |
| B. | 9.0 g草酸被NaClO氧化生成CO2,转移的电子数为0.2 NA | |
| C. | 9.0 g草酸溶于水,其中C2O42-和HC2O4-的微粒数之和为0.1NA | |
| D. | 9.0g草酸受热完全分解为CO2、CO、H2O,标况下测得生成的气体体积为4.48 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com