

| A、图Ⅰ表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B、图Ⅱ表示常温下,0.1000mol/LNaOH溶液滴定20.00mL、0.100mol/LHCl溶液所得到的滴定曲线 |
| C、图Ⅲ表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c<a<b |
| D、图Ⅳ表示反应4CO(g)+2NO2(g)?N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c>b>a |


科目:高中化学 来源: 题型:
 有等质量的A、B两金属的粉末,相对原子质量Ar(A)<Ar(B),将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如图.下列说法不正确的是( )
有等质量的A、B两金属的粉末,相对原子质量Ar(A)<Ar(B),将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如图.下列说法不正确的是( )| A、金属活动性强弱:A>B |
| B、反应后A、B可能都有剩余 |
| C、消耗B的质量一定小于A的质量 |
| D、消耗的稀硫酸和稀盐酸质量一定不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
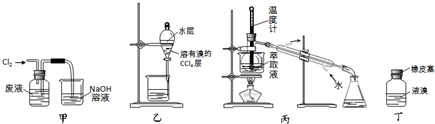
| A、用装置甲氧化废液中的溴化氢 |
| B、用装置乙分离油层和水层 |
| C、用装置丙分离四氯化碳和液溴 |
| D、用仪器丁密封存放单质溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:
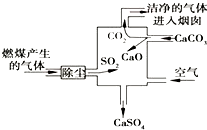
| A、进入烟囱的气体为纯净物 |
| B、此过程中硫元素的化合价没有发生改变 |
| C、使用此废气处理装置可减少酸雨的形成 |
| D、整个过程的反应可表示为:2SO2+2CaCO3+O2═2CaSO4+2CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 现象或反应 | 原理解释 |
| A | AgCl沉淀中滴入少量KI溶液有黄色沉淀生成 | Ksp(AgI)>Ksp(AgCl) |
| B | 将AlCl3溶液加入到过量的氨水中有白色沉淀生成 | Al(OH)3不溶于碱 |
| C | 电解饱和食盐水没有Cl2放出 | 阳极可能没有选择惰性材料 |
| D | 向无色溶液中滴加盐酸有白色沉淀生成 | 该溶液中一定含有Ag+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序 号 | ① | ② | ③ | ④ |
| 溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
| pH | 7.0 | 7.0 | 8.1 | 8.4 |
| A、酸的强度:HF>H2CO3 |
| B、由水电离产生的c(H+):①=② |
| C、溶液中离子的总浓度:①>③ |
| D、④溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)=1mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
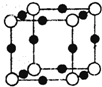 氧是地壳中含量最高的非金属元素,铝是地壳中含量最高的金属元素,氮是空气中含量最高的元素.
氧是地壳中含量最高的非金属元素,铝是地壳中含量最高的金属元素,氮是空气中含量最高的元素.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com