
【题目】在298 K、1.01×105 Pa,将22 g CO2通入0.75 L 1.0 mol·L-1NaOH溶液中充分反应,测得反应放出的热量为a kJ。已知该条件下1 mol CO2通入1 L 2.0 mol·L-1NaOH溶液中充分反应放出的热量为b kJ。则CO2与NaOH反应生成NaHCO3的热化学方程式为( )。
A. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=-(2b-a) kJ·mol-1
NaHCO3(aq) ΔH=-(2b-a) kJ·mol-1
B. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=+(4a-b) kJ·mol-1
NaHCO3(aq) ΔH=+(4a-b) kJ·mol-1
C. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1
NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1
D. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=+(2b-a) kJ·mol-1
NaHCO3(aq) ΔH=+(2b-a) kJ·mol-1
【答案】C
【解析】
根据题意可知,22gCO2通入1molL-1NaOH溶液750mL中充分反应,测得反应放出akJ的热量,写出热化学反应方程式,再利用1molCO2通入2molL-1NaOH溶液1L中充分反应放出bkJ的热量写出热化学反应方程式,最后利用盖斯定律来书写CO2与NaOH溶液反应生成NaHCO3的热化学方程式。
根据题意,22gCO2通入1molL-1NaOH溶液750mL中充分反应,n(CO2)=![]() =0.5mol,n(NaOH)=1molL-1×0.75L=0.75mol,该反应既生成碳酸钠又生成碳酸氢钠,方程式为2CO2+3NaOH═NaHCO3+Na2CO3+H2O,由0.5molCO2反应放出热量为aKJ,则2molCO2反应放出热量为4aKJ,即热化学反应方程式为2CO2(g)+3NaOH(aq)═NaHCO3(aq)+Na2CO3(aq)+H2O(l)△H=-4aKJ/mol①。又1molCO2通入2molL-1NaOH溶液1L中充分反应放出bkJ的热量,则热化学方程式为2NaOH(aq)+CO2(g)═Na2CO3(aq)+H2O(l)△H=-bKJ/mol②,由盖斯定律可知,①-②可得,CO2(g)+NaOH(aq)
=0.5mol,n(NaOH)=1molL-1×0.75L=0.75mol,该反应既生成碳酸钠又生成碳酸氢钠,方程式为2CO2+3NaOH═NaHCO3+Na2CO3+H2O,由0.5molCO2反应放出热量为aKJ,则2molCO2反应放出热量为4aKJ,即热化学反应方程式为2CO2(g)+3NaOH(aq)═NaHCO3(aq)+Na2CO3(aq)+H2O(l)△H=-4aKJ/mol①。又1molCO2通入2molL-1NaOH溶液1L中充分反应放出bkJ的热量,则热化学方程式为2NaOH(aq)+CO2(g)═Na2CO3(aq)+H2O(l)△H=-bKJ/mol②,由盖斯定律可知,①-②可得,CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1,故C正确;
NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1,故C正确;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】利用下列实验装置不能完成相应实验的是( )

A. 用装置①测量生成氧气的化学反应速率
B. 用装置②比较NaHCO3和Na2CO3的热稳定性
C. 装置③中分液漏斗内的液体可顺利加入蒸馏烧瓶
D. 装置④可实现制取CO2实验中的“即关即止,即开即用”的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据《天工开物》记载,我国古代以炉甘石(主要成分是ZnCO3)来升炼倭铅(即锌),其原理如图。已知锌的熔点420 ℃、沸点906 ℃。则下列说法不正确的是

A. 升炼倭铅过程包含分解反应和氧化还原反应
B. 冶炼时锌变为蒸气在兜室冷凝为固体
C. “泥封”的目的是为了防止得到的锌被氧化
D. “锌火”是锌蒸气和一氧化碳在空气的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池充电时间短,续航能力强,其充放电原理为VO2++V3++H2O![]() VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是
VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是

A. 全钒液流电池放电时,正极的电极反应式为VO2++2H++e-=VO2++H2O
B. 图中a电极为阴极,N物质是H2
C. 全钒液流电池充电时,V3+被氧化为VO2+
D. 电解时,b电极的反应式为SO32-+H2O-2e-=SO42-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)。在密闭容器中发生该反应时
2CO2(g)+N2(g)。在密闭容器中发生该反应时
,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
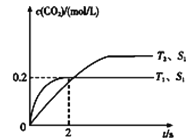
据此判断:
①该反应的温度T2____ T1 (填“>”或“<”)。
②在T1温度下,0~2 s内的平均反应速率v(N2)=___________。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若增大催化剂的表面积,则CO转化率__ (填“增大”“减小”或“不变”)。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____(填字母)。
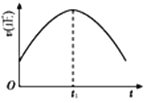
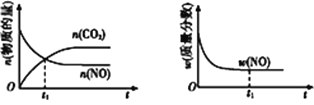
a b c
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-867.0 kJ/mol
2NO2(g)![]() N2O4(g) ΔH=-56.9 kJ/mol
N2O4(g) ΔH=-56.9 kJ/mol
写出CH4催化还原N2O4(g)生成N2、CO2和H2O(g)的热化学方程式:_________________。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极a、b表面发生的电极反应式分别为a:____________________,
b:___________________________________。
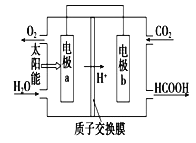
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)在5L密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v为
4NO(g)+6H2O(g)在5L密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v为
A. v(O2)=0.01mol/(L·s) B. v(NO)=0.08mol/(L·s)
C. v(H2O)=0.003mol/(L·s) D. v(NH3)=0.001mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化曲线如图所示。下列因素中,影响该反应速率的主要因素是

①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A. ①④ B. ③④ C. ①③ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
![]()
(1)写出A、B、C三元素名称_______、_______、_______。
(2)C在元素周期表中的位置是___________________。
(3)B的原子结构示意图为______。C的氢化物与B的氢化物的稳定性强弱顺序为(填化学式)___________。
(4)比较A、C的原子半径A____C。写出A的气态氢化物与A的最高价氧化物对应水化物反应的化学方程式_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com