
| A£® | ĘäĖūĢõ¼ž²»±ä£¬ČōĘšŹ¼Ź±¼ÓČė1molxŗĶ2molY£¬ŌņĘ½ŗāŹ±ZµÄĪļÖŹµÄĮæČŌĪŖ0.5mol | |
| B£® | ĘäĖūĢõ¼ž²»±ä£¬ŌŁĻņČŻĘ÷ÖŠ¼ÓČė2 mol XŗĶ1 mol Y£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬Ę½ŗāŹ±X”¢YµÄ×Ŗ»ÆĀŹŌö“ó | |
| C£® | ĘäĖūĢõ¼ž²»±ä£¬ÉżøßŅ»¶ØĪĀ¶Čŗó£¬øĆ·“Ó¦Ę½ŗā³£ŹżK=2.0£¬Ōņ”÷H£¾0 | |
| D£® | ŅŌxÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ0.01 mol/£ØL•min£© |
·ÖĪö X£Øg£©+Y£Øg£©?Z£Øg£©
³õŹ¼£Ømol£©2 1 0
×Ŗ»Æ£Ømol£©0.5 0.5 0.5
Ę½ŗā£Ømol£©1.5 0.5 0.5
Ę½ŗāŹ±ø÷×é·ÖµÄÅØ¶Č·Ö±šĪŖ£ŗc£ØX£©=$\frac{1.5mol}{5L}$0.3mol/L”¢c£ØY£©=$\frac{0.5mol}{5L}$=0.1mol/L”¢c£ØZ£©=$\frac{0.5mol}{5L}$=0.1mol/L£¬øĆĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ£ŗK=$\frac{0.1}{0.3”Į0.1}$=$\frac{10}{3}$£¬
A£®ĪĀ¶Č²»±ä£¬ŌņøĆ·“Ó¦µÄĘ½ŗā³£Źż²»±ä£¬X”¢Y”¢ZµÄ¼ĘĮæŹżÓÖĻąµČ£¬Ōņ¼ÓČė2molXŗĶ1mol YÓė¼ÓČė1molXŗĶ2molY£¬“ļµ½Ę½ŗāŹ±ZµÄĪļÖŹµÄĮæ²»±ä£»
B£®ŌŁĻņČŻĘ÷ÖŠ¼ÓČė2 molXŗĶ1 molY£¬Ļąµ±ÓŚŌö“óĮĖŃ¹Ēæ£¬Ę½ŗāĻņ×ÅÕżĻņŅĘ¶Æ£»
C£®ĻČøł¾Ż»ÆŃ§Ę½ŗāµÄČż¶ĪŹ½¼ĘĖć³öĘ½ŗāÅØ¶Č£¬Č»ŗó¼ĘĖć³öøĆ·“Ó¦ŌŚøĆĪĀ¶ČĻĀµÄĘ½ŗā³£Źż£¬øł¾ŻĘ½ŗā³£Źż±ä»ÆÅŠ¶ĻøĆ·“Ó¦µÄģŹ±ä£»
D£®øł¾Żv=$\frac{\frac{”÷n}{V}}{”÷t}$¼ĘĖć³öŅŌXÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹ£®
½ā“š ½ā£ŗX£Øg£©+Y£Øg£©?Z£Øg£©
³õŹ¼£Ømol£©2 1 0
×Ŗ»Æ£Ømol£©0.5 0.5 0.5
Ę½ŗā£Ømol£©1.5 0.5 0.5
Ę½ŗāŹ±ø÷×é·ÖµÄÅØ¶Č·Ö±šĪŖ£ŗc£ØX£©=$\frac{1.5mol}{5L}$0.3mol/L”¢c£ØY£©=$\frac{0.5mol}{5L}$=0.1mol/L”¢c£ØZ£©=$\frac{0.5mol}{5L}$=0.1mol/L£¬øĆĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ£ŗK=$\frac{0.1}{0.3”Į0.1}$=$\frac{10}{3}$£¬
A£®ĪĀ¶Č²»±ä£¬ŌņøĆ·“Ó¦µÄĘ½ŗā³£Źż²»±ä£¬X”¢Y”¢ZµÄ¼ĘĮæŹżÓÖĻąµČ£¬Ōņ¼ÓČė2molXŗĶ1mol YÓė¼ÓČė1molXŗĶ2molY£¬“ļµ½Ę½ŗāŹ±ZµÄĪļÖŹµÄĮæ²»±ä£¬¼“Ę½ŗāŹ±ZµÄĪļÖŹµÄĮæČŌĪŖ0.5mol£¬¹ŹAÕżČ·£»
B£®ĘäĖūĢõ¼ž²»±ä£¬ŌŁĻņČŻĘ÷ÖŠ¼ÓČė2 molXŗĶ1 molY£¬Ļąµ±ÓŚŌö“óĮĖŃ¹Ēæ£¬Ę½ŗāĻņ×ÅÕżĻņŅĘ¶Æ£¬ŌņĘ½ŗāŹ±X”¢YµÄ×Ŗ»ÆĀŹŌö“󣬹ŹBÕżČ·£»
C£®ÉżøßŅ»¶ØĪĀ¶Čŗó£¬øĆ·“Ó¦Ę½ŗā³£ŹżK=2.0£¼$\frac{10}{3}$£¬ĖµĆ÷ÉżøßĪĀ¶ČĘ½ŗāĻņ×ÅÄęĻņŅĘ¶Æ£¬ŌņøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬øĆ·“Ó¦µÄģŹ±ä”÷H£¼0£¬¹ŹCÕżČ·£»
D£®Ę½ŗāŹ±ÓĆX±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ£ŗv£ØX£©=$\frac{\frac{0.5mol}{5L}}{1min}$=0.1mol/£ØL•min£©£¬¹ŹD“ķĪó£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·»ÆŃ§Ę½ŗā¼°ĘäÓ°ĻģŅņĖŲĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕČż¶ĪŹ½ŌŚ»ÆŃ§Ę½ŗā¼ĘĖćÖŠµÄÓ¦ÓĆ£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°»Æѧ¼ĘĖćÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 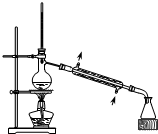 “ÓĆŗ½¹ÓĶÖŠĢįČ”±½ | B£® | 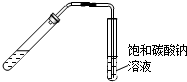 ŹµŃéŹŅÖĘŅŅĖįŅŅõ„ | ||
| C£® | 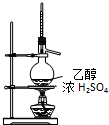 ŹµŃéŹŅÖĘŅŅĻ© | D£® | 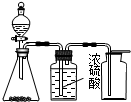 ŹµŃéŹŅÖĘČ””¢ŹÕ¼ÆŅŅČ²ĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
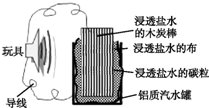 ĄūÓĆÉś»īÖŠ³£¼ūµÄ²ÄĮĻæÉŅŌ½ųŠŠŗܶąæĘѧŹµŃ飬ĻĀĶ¼¾ĶŹĒŅ»øöÓĆ·Ļ¾É²ÄĮĻÖĘ×÷µÄæÉÓĆÓŚĒż¶ÆĶę¾ßµÄµē³ŲµÄŹ¾ŅāĶ¼£®µ±µē³Ų¹¤×÷Ź±£¬ÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
ĄūÓĆÉś»īÖŠ³£¼ūµÄ²ÄĮĻæÉŅŌ½ųŠŠŗܶąæĘѧŹµŃ飬ĻĀĶ¼¾ĶŹĒŅ»øöÓĆ·Ļ¾É²ÄĮĻÖĘ×÷µÄæÉÓĆÓŚĒż¶ÆĶę¾ßµÄµē³ŲµÄŹ¾ŅāĶ¼£®µ±µē³Ų¹¤×÷Ź±£¬ÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | ĀĮ¹Ž²»»į±»øÆŹ“ | |
| B£® | ľĢæ°ōÉĻ·¢ÉśµÄ·“Ó¦ĪŖO2+2H2O+4e-ØT4OH- | |
| C£® | ľĢæ°ōÓ¦ÓėĶę¾ßµē»śµÄøŗ¼«ĻąĮ¬ | |
| D£® | øƵē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗóľĢæ°ōŗĶĢ¼Į£µÄÖŹĮæ»į¼õĒį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol¹ĢĢåSµ„ÖŹČ¼ÉշųöµÄČČĮæ“óÓŚ293.23 kJ | |
| B£® | 1molĘųĢåSµ„ÖŹČ¼ÉշųöµÄČČĮæŠ”ÓŚ293.23 kJ | |
| C£® | 1 mol SO2£Øg£©µÄ¼üÄܵÄ×ÜŗĶ“óÓŚ1 mol S£Øl£©ŗĶ1 mol O2£Øg£©µÄ¼üÄÜÖ®ŗĶ | |
| D£® | 1 mol SO2£Øg£©µÄ¼üÄܵÄ×ÜŗĶŠ”ÓŚ1 mol S£Øl£©ŗĶ1 mol O2£Øg£©µÄ¼üÄÜÖ®ŗĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
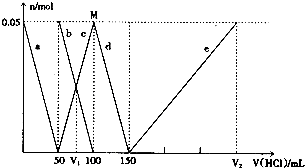
| A£® | V1£ŗV2=l£ŗ5 | |
| B£® | MµćŹ±Éś³ÉµÄCO2ĪŖ0.05mol | |
| C£® | Ō»ģŗĻČÜŅŗÖŠµÄCO32-ÓėAlO2-µÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ2 | |
| D£® | aĒśĻß±ķŹ¾µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗAlO2-+H++H2OØTAl£ØOH£©3”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
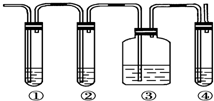 ŹµŃéŹŅÖĘČ”ŅŅĻ©£¬³£ŅņĪĀ¶Č¹żø߶ųŹ¹ŅŅ“¼ŗĶÅØĮņĖį·“Ӧɜ³ÉÉŁĮæµÄ¶žŃõ»ÆĮņ£®ÓŠČĖÉč¼ĘĻĀĮŠŹµŃéŅŌČ·ČĻÉĻŹö»ģŗĻĘųĢåÖŠÓŠŅŅĻ©ŗĶ¶žŃõ»ÆĮņ£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
ŹµŃéŹŅÖĘČ”ŅŅĻ©£¬³£ŅņĪĀ¶Č¹żø߶ųŹ¹ŅŅ“¼ŗĶÅØĮņĖį·“Ӧɜ³ÉÉŁĮæµÄ¶žŃõ»ÆĮņ£®ÓŠČĖÉč¼ĘĻĀĮŠŹµŃéŅŌČ·ČĻÉĻŹö»ģŗĻĘųĢåÖŠÓŠŅŅĻ©ŗĶ¶žŃõ»ÆĮņ£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶£ŗR£¾Z£¾Y | |
| B£® | XµÄ×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļ·Ö×ÓÖŠŗ¬ÓŠ18øöµē×Ó | |
| C£® | YÓėZŠĪ³ÉµÄ³£¼ū»ÆŗĻĪļ¼ČÄÜÓėĖį·“Ó¦£¬ÓÖÄÜÓė¼ī·“Ó¦ | |
| D£® | Ķ¬ÖÜĘŚŌŖĖŲÖŠRµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ×īĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| »ÆѧŹ½ | NH4NO3 | NaOH | NaCl | KNO3 |
| ČܽāČČ£ØkJ/kg£© | -330.75 | +1040.5 | -84.10 | -353.17 |
| A£® | NH4NO3 | B£® | NaOH | C£® | NaCl | D£® | KNO3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com