

分析 (1)根据n=cV计算出碳酸钾的物质的量,根据n=$\frac{V}{{V}_{m}}$计算出二氧化碳的物质的量,结合二者物质的量判断反应后产物,然后计算出其物质的量及浓度;
(2)该富液中溶质组成为K2CO3 0.75 mol/L、KHCO3 1.5 mol/L,溶液呈碱性,结合电荷守恒、物料守恒判断;
(3)碳酸氢钾加热分解生成碳酸钾、二氧化碳气体和水,据此写出反应的化学方程式;
(4)根据电解原理及阴阳两极发生的反应原理分析.
解答 解:(1)标准状况下3.36L二氧化碳的物质的量为:$\frac{3.36L}{22.4L/mol}$=0.15mol,200mL 1.5mol/L K2CO3溶液中含有碳酸钾的物质的量为:1.5mol/L×0.2L=0.3mol,0.5mol二氧化碳完全反应消耗0.15mol碳酸钾,生成了0.3mol碳酸氢钾KHCO3,则反应后溶质为KHCO3、K2CO3,浓度为:c(K2CO3)=$\frac{0.3mol-0.15mol}{0.2L}$=0.75mol/L;KHCO3的浓度为:c(KHCO3)=$\frac{0.3mol}{0.2L}$=1.5mol/L,
故答案为:K2CO3 0.75 mol/L、KHCO3 1.5 mol/L;
(2)a.溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒可知:c(K+)>2c(CO32-)+c(HCO3-),故a错误;
b.根据物料守恒可得:3c(K+)=4c(CO32-)+4c(HCO3-)+4c(H2CO3),故b正确;
c.溶质组成为K2CO3 0.75 mol/L、KHCO3 1.5 mol/L,由于水解程度较小,则c(HCO3-)>c(CO32-)、c(OH-)>c(H+),溶液中离子浓度大小为:c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故c正确;
故答案为:bc;
(3)碳酸氢钾加热分解生成碳酸钾、二氧化碳气体和水,反应的化学方程式为:2KHCO3$\frac{\underline{\;\;△\;\;}}{\;}$K2CO3+CO2↑+H2O,
故答案为:2KHCO3$\frac{\underline{\;\;△\;\;}}{\;}$K2CO3+CO2↑+H2O;
(4)由于OH-在阳极失电子生成O2(4OH--4e-═O2↑+2H2O),产生的H+消耗溶液中的HCO3-(H++HCO3-═CO2↑+H2O);在阴极室中的HCO3-、CO32-进入阳极室,发生反应CO32-+CO2+H2O═2HCO3-或CO32-+H+═HCO3-,使HCO3-得以补充,溶液组成和浓度基本不变,
故答案为:OH-在阳极失电子生成O2(4OH--4e-═O2↑+2H2O),产生的H+消耗溶液中的HCO3-(H++HCO3-═CO2↑+H2O);阴极室中的HCO3-、CO32-进入阳极室,发生反应CO32-+CO2+H2O═2HCO3-或CO32-+H+═HCO3-,使HCO3-得以补充,溶液组成和浓度基本不变.
点评 本题考查了离子浓度大小比较,题目难度中等,涉及电解原理、盐的水解原理、化学方程式计算、离子浓度大小比较等知识,明确电解原理、电荷守恒、物料守恒为解答根据,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ③④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是表示原子、分子、离子的物理量 | |
| B. | 摩尔质量就是相对分子质量 | |
| C. | 1mol任何粒子的粒子数叫做阿伏伽德罗常数,符号为NA | |
| D. | 物质的量就是物质的质量或数量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气能使干燥的有色布条褪色 | |
| B. | 能使湿润的淀粉KI 试纸变蓝的物质一定是氯气 | |
| C. | 电解饱和食盐水可制得氯气 | |
| D. | 氯原子和氯离子的化学性质相似,都具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将一定量KAl(SO4)2溶液和一定量Ba(OH)2溶液混合,沉淀的质量恰好最大时:Al3++2SO42-+3OH-+2Ba2+=2BaSO4↓+Al(OH)3↓ | |
| B. | KMnO4与浓盐酸反应制Cl2:2MnO4-+16HCl=2Mn2++6Cl-+5Cl2↑+8H2O | |
| C. | 0.1molCl2和100mL1mol/LFeBr2反应:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2 | |
| D. | 用Al(OH)3中和过多的胃酸:Al(OH)3+3H+=Al3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
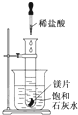 如图所示,把盛有几小块镁片的试管放入盛有25℃的饱和石灰水的烧杯中,再用滴管向试管中滴入2mL的稀盐酸.下列对烧杯中的实验现象的描述及原因说明中正确的是( )
如图所示,把盛有几小块镁片的试管放入盛有25℃的饱和石灰水的烧杯中,再用滴管向试管中滴入2mL的稀盐酸.下列对烧杯中的实验现象的描述及原因说明中正确的是( )| A. | 烧杯中出现白色浑浊,原因是试管中的反应放出热量使烧杯中饱 和石灰水温度升高,溶质析出 | |
| B. | 烧杯中出现白色浑浊,原因是试管中的反应吸收热量使烧杯中饱和石灰水温度降低,溶质析出 | |
| C. | 烧杯中没有任何现象,原因是试管中的反应与烧杯中饱和石灰水没有关系 | |
| D. | 烧杯中没有任何现象,原因是试管中的反应既不放出热量,也不吸收热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com